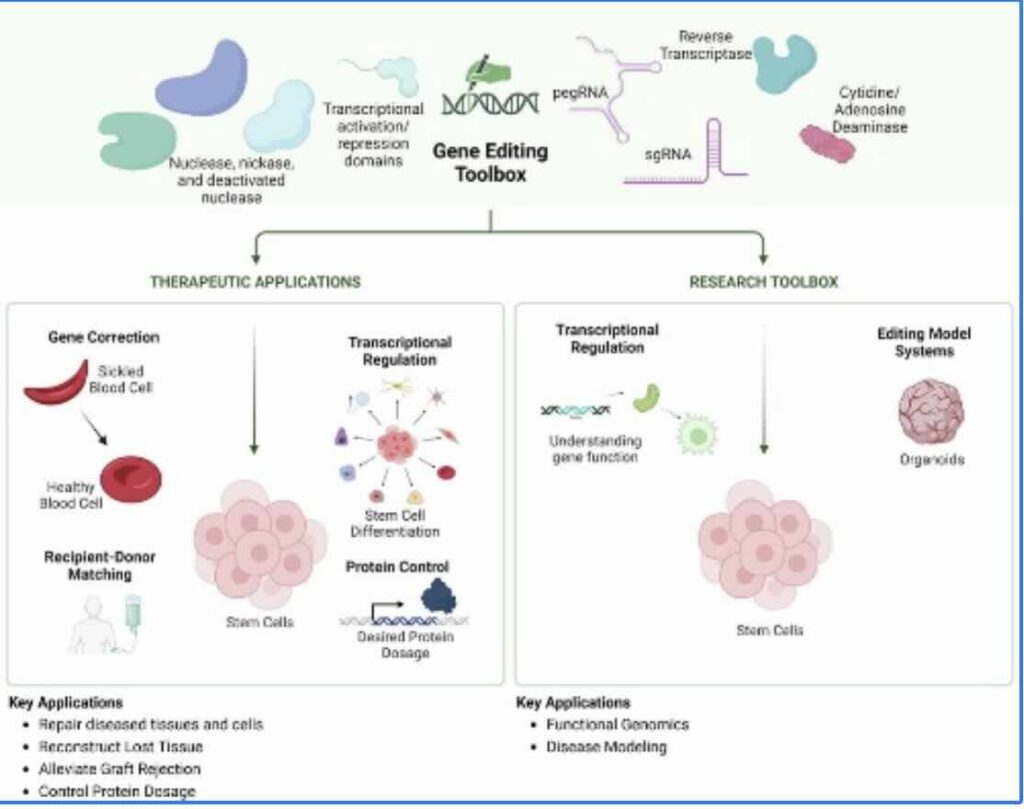
Er zijn nog heel wat hindernissen weg te nemen voor de toepassing van de CRISPR-methode in de regeneratieve geneeskunde (afb: Kam Leong et al./Tissue Engineering)
Regeneratieve geneeskunde richt zich op het herstellen of vervangen van beschadigd weefsel en organen en biedt daarmee hoop aan patiënten met verschillende aandoeningen. Traditionele strategieën, zoals het gebruik van voorlopercellen en biologische stimuli, hebben enig succes gehad, maar ze kampen met beperkingen zoals onbedoelde veranderingen en een gebrek aan precisie. Genoombewerking, met name op CRISPR/Cas9 gebaseerde systemen, biedt een nauwkeuriger en efficiënter alternatief, maar voorlopig is die aanpak nog lang niet vrij van mankementen en zal voorlopig nog wel een (dure) belofte blijven. Lees verder

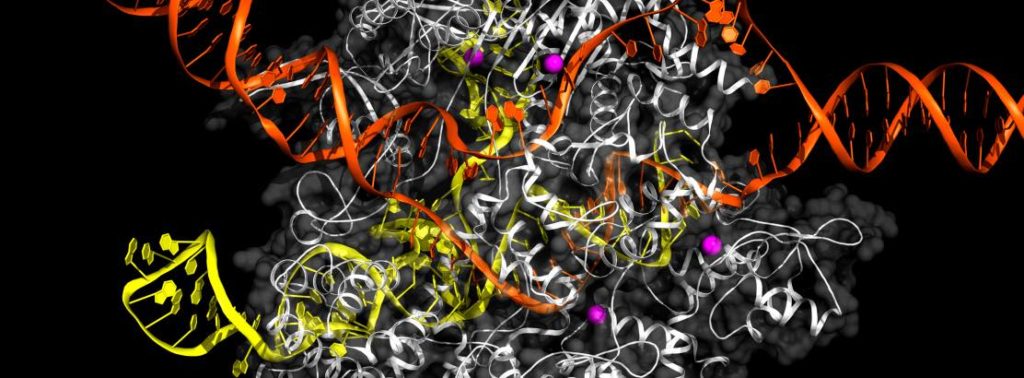
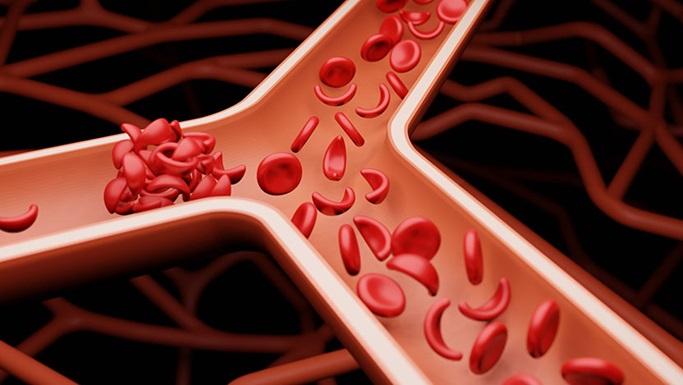
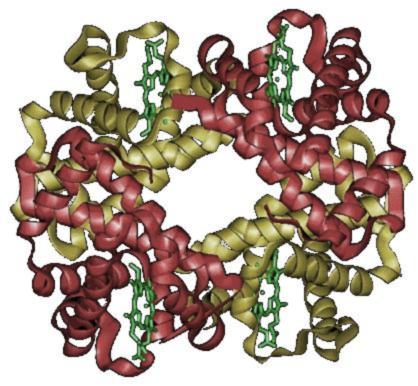




 Gentherapieën zijn al jaren een belofte om genetische aberraties te herstellen, maar proeven daarmee bleken ook vaak op te lopen tegen niet voorziene problemen. Het lijkt er op dat er nu zo langzamerhand een paar ‘winnaars’ zijn komen bovendrijven al is het ook daar nog allesbehalve koek en ei. Sommige behandelingen werken wel, maar halen de oorzaak niet weg en verreweg de meeste (misschien wel alle) genbehandelingen zijn vreselijk duur. We hebben het dan over honderdduizenden of zelfs miljoenen euro’s (eigenlijk dollars), schrijft Nature en een verhaal over min of meer succesvolle therapieën. Het blad geeft vier voorbeelden daarvan. Uitsluitend Amerikaans, overigens
Gentherapieën zijn al jaren een belofte om genetische aberraties te herstellen, maar proeven daarmee bleken ook vaak op te lopen tegen niet voorziene problemen. Het lijkt er op dat er nu zo langzamerhand een paar ‘winnaars’ zijn komen bovendrijven al is het ook daar nog allesbehalve koek en ei. Sommige behandelingen werken wel, maar halen de oorzaak niet weg en verreweg de meeste (misschien wel alle) genbehandelingen zijn vreselijk duur. We hebben het dan over honderdduizenden of zelfs miljoenen euro’s (eigenlijk dollars), schrijft Nature en een verhaal over min of meer succesvolle therapieën. Het blad geeft vier voorbeelden daarvan. Uitsluitend Amerikaans, overigens