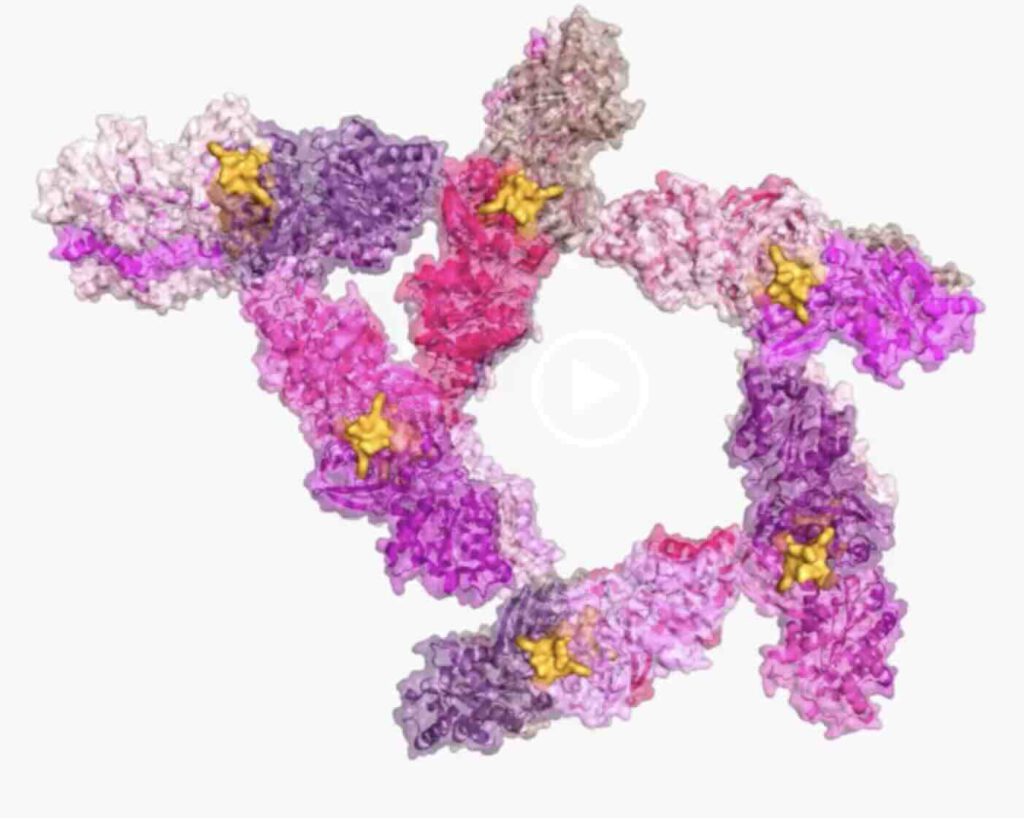
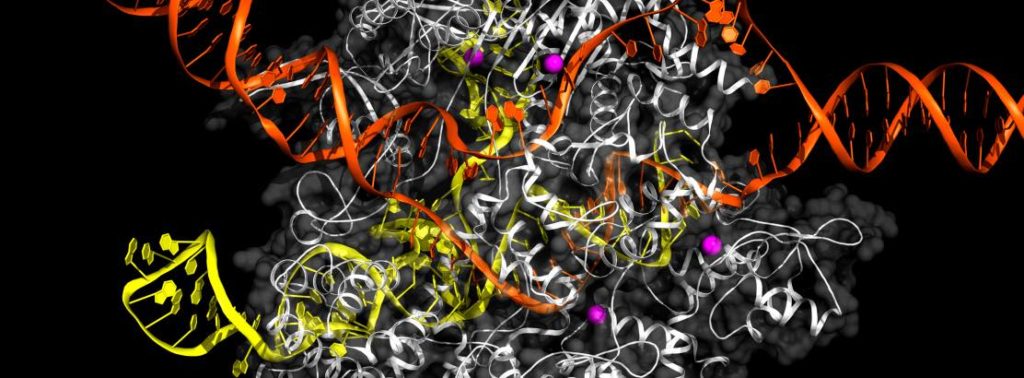
CARF-effectoren, hier Cat1 (denk ik=as), maken het bacteriofagen onmogelijk zich te vermenigvuldigen (afb: Rockefelleruniversiteit)
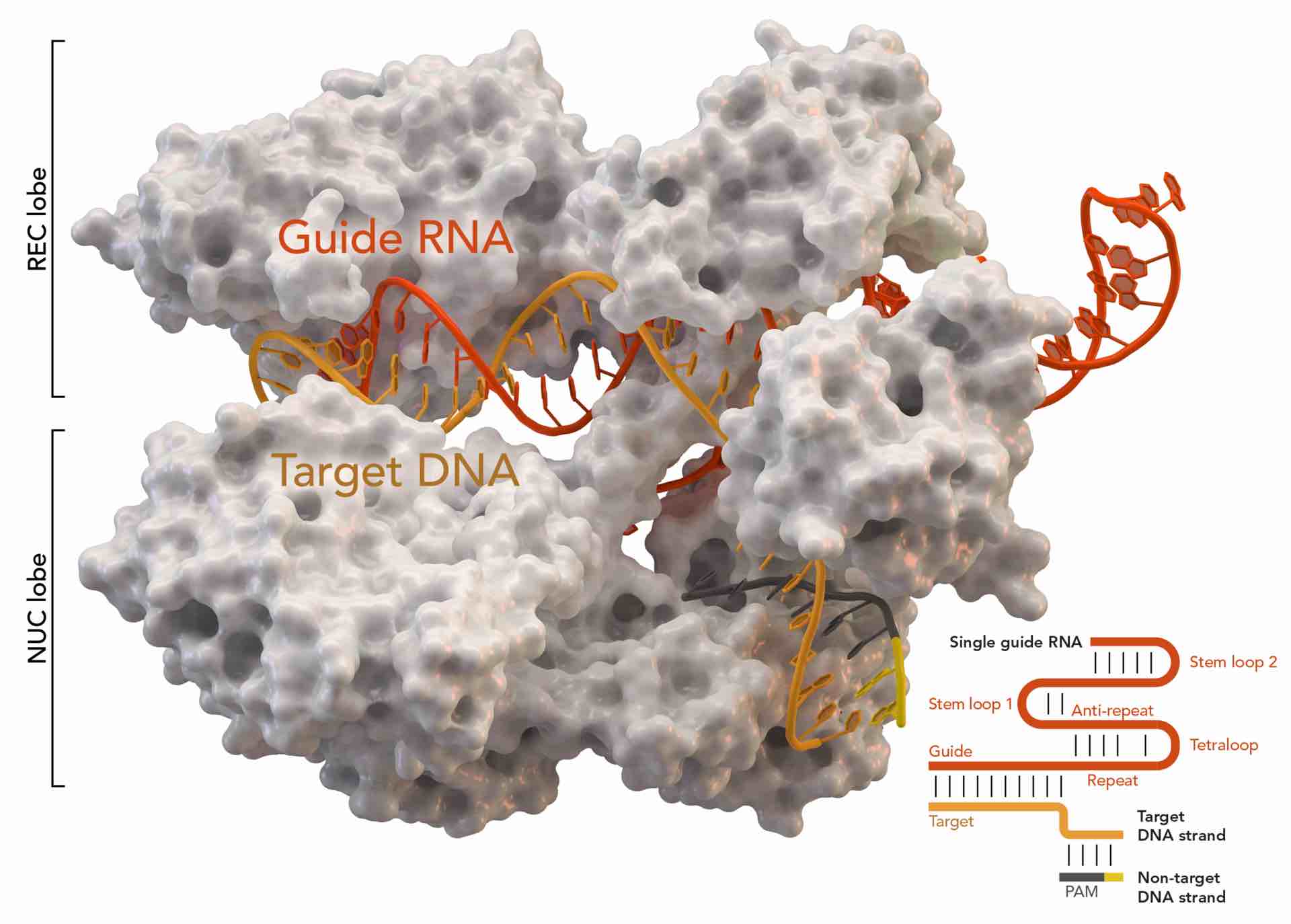
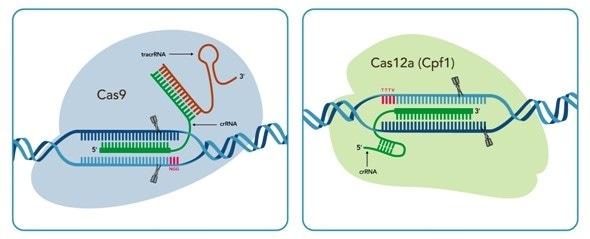
Elk levend organisme op aarde moet zichzelf beschermen tegen dingen die het kwaad kunnen doen. Bacteriën zijn daarop geen uitzondering en ondanks hun relatieve eenvoud, zetten ze opmerkelijk slimme verdedigingsstrategieën in tegen virale indringers. De bekendste is CRISPR/Cas9 die nu ook gebruikt wordt voor onderzoek, maar ook voor het ‘repareren’ van ziekmakende genetische afwijkingen. Er zijn nog andere bacteriële afweermechanismen tegen virussen en er is (dus) nog veel te ontdekken. Die zogeheten CARF-effectoren van bacteriën lijken me(=as) overigens vooral ‘wapens’ tegen virale infecties en hebben weinig met genoombewerking te maken. Lees verder

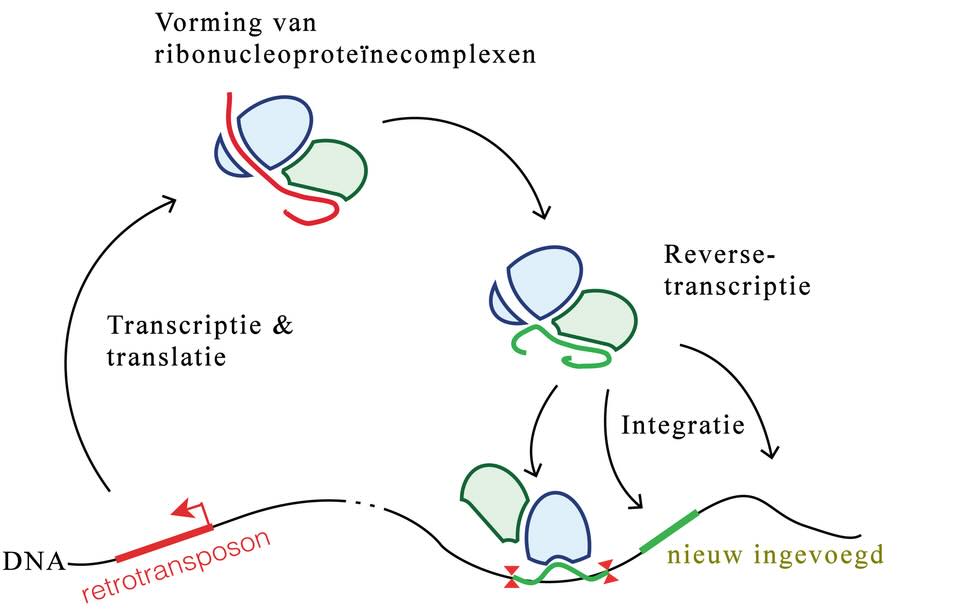

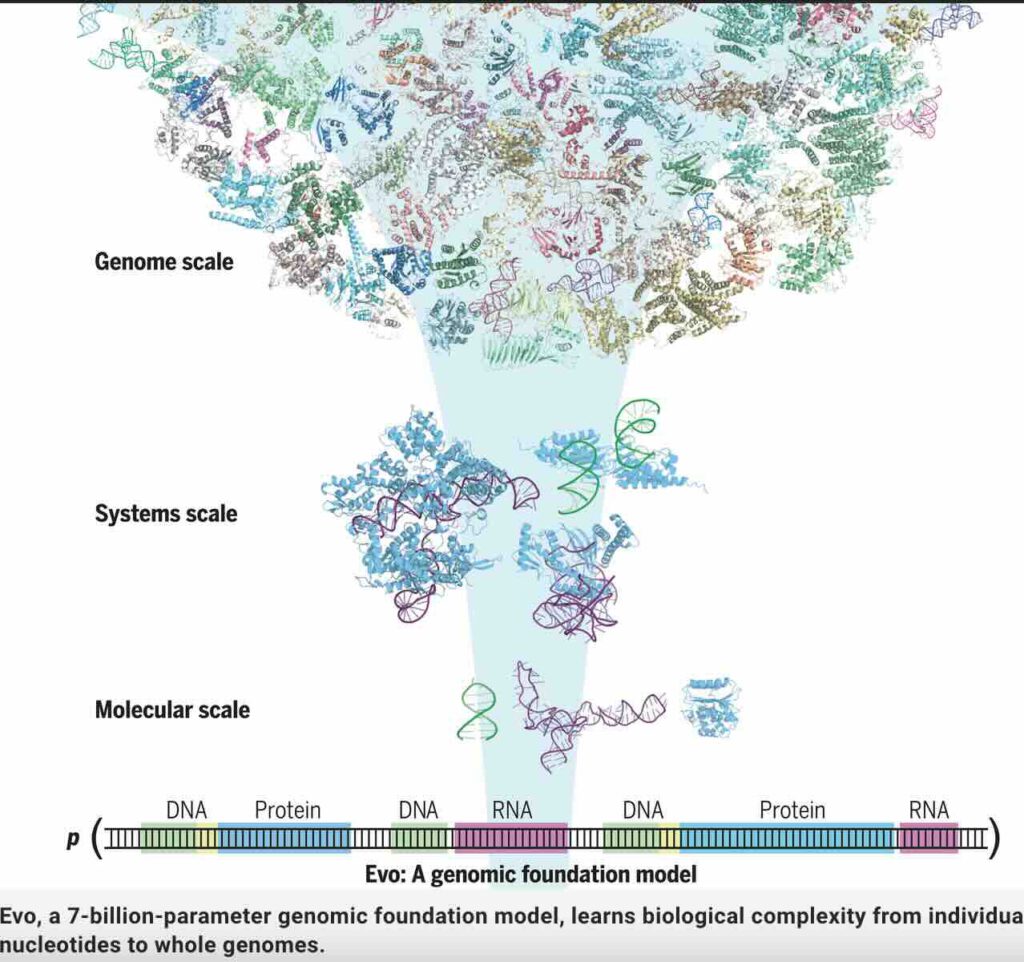 Onderzoekers van de Stanforduniversiteit rond
Onderzoekers van de Stanforduniversiteit rond