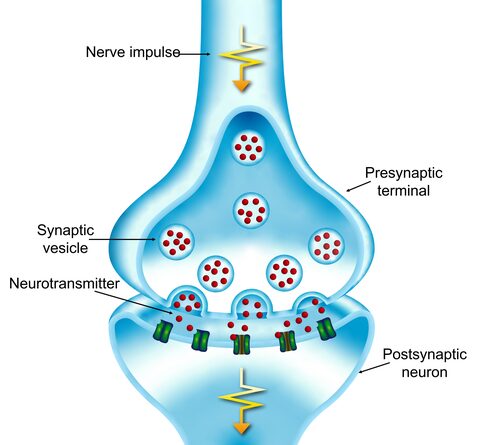
De signaaloverdracht via synapsen van buurcellen in de hersens (afb: OIST)


De signaaloverdracht via synapsen van buurcellen in de hersens (afb: OIST)
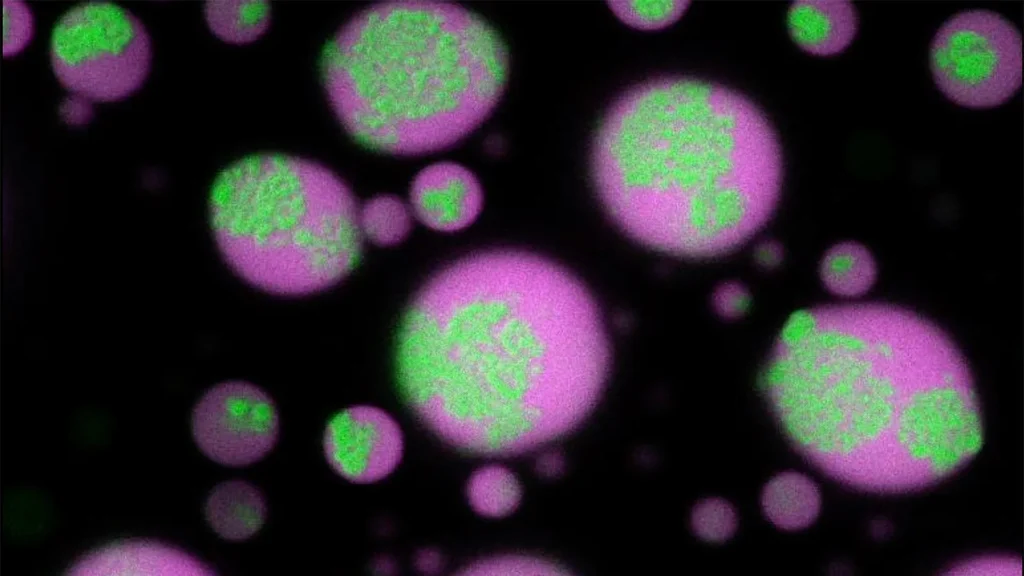
RNA-klonteringen(groen) vallen geleidelijk uiteen in biomoleculaire condensaten (magenta), waardoor het RNA weer oplosbaar wordt. Dit gebeurde nadat een antisense-oligonucleotide, ontwikkeld door het team van Priya Banerjee, aan het condensaat werd toegevoegd. (afb: Universiteit van Buffalo)
Wetenschappers hebben ontdekt hoe bepaalde eiwitklonteringen in de hersens ontstaan en hebben ook een oplossing daarvoor bedacht. en laten ze verdwijnen. Eiwitklonteringen in de hersens komen voor bij de ziektes van Alzheimer, van Parkinson en naar het schijnt (ik=as was me er niet van bewust) ook bij ALS (amyotrofe laterale sclerose) en de ziekte van Huntington.
Bij de laatste twee ziektes gaat het om kleverige RNA-kluwens die kleine vloeistofachtige druppeltjes vormen in cellen en die lang kunnen blijven bestaan, ook nadat hun omgeving is verdwenen. Door introductie van het kleverige eiwit G3BP1, konden de onderzoekers de vorming van de RNA-klonteringen stoppen en met een speciaal ontworpen stukje RNA (ASO, in afko) konden ze die zelfs oplossen. Overigens is het mij niet duidelijk wat de verwijdering van die klonteringen voor de ziek(t)e betekent. Lees verder
Caveoline-1 (groene sliertjes) zouden de schade in hersencellen bij, onder meer, Alzheimer en Parkinson kunnen herstellen (afb: eikonoklastes.com/)
Onderzoekers van de universiteit van Californië in San Diego hebben een gentherapie voor de ziekte van Alzheimer ontwikkeld die de hersenen kan helpen beschermen tegen schade en de cognitieve functie kan behouden. In tegenstelling tot bestaande behandelingen voor Alzheimer die zich richten op ongezonde eiwitafzettingen in de hersenen, zou de nieuwe aanpak kunnen helpen de onderliggende oorzaak van Alzheimer aan te pakken door het gedrag van de hersencellen zelf te beïnvloeden. In die therapie speelt het eiwit caveoline-1 een belangrijke rol. Lees verder
Twee recente klinische studies (fase I (VS) en fase I en II (Japan)) maken aannemelijk dat na transplantatie van voorlopercellen van dopamineneuronen rechtstreeks in de hersenen die cellen daar kunnen overleven, dopamine kunnen produceren en motorische symptomen van Parkinsonpatiënten aanzienlijk kunnen verminderen. Fase I van een klinische proef gaat vooral om de veiligheid van methode vast te stellen. De resultaten zijn dus nog zeer voorlopig, ook al omdat het aantal proefpersonen vrij beperkt was (resp. twaalf en zeven). Lees verder

Een opengewerkte mitochondrion
Nieuw onderzoek naar de oorzaken van de fatale spier ziekte amyotrofe laterale sclerose (ALS) opent mogelijk de deur naar vroegtijdige behandeling. De onderzoeksters zouden een ‘schuldige’ hebben kunnen aanwijzen bij verschillende mutaties die (kunnen) leiden tot de ziekte. Het lijkt er op dat de ziekte begint in de mitochondriën van zenuwcellen, nog voor de symptomen van de ziekte verschijnen. Vooralsnog is de ziekte niet of nauwelijks behandelbaar. Lees verder
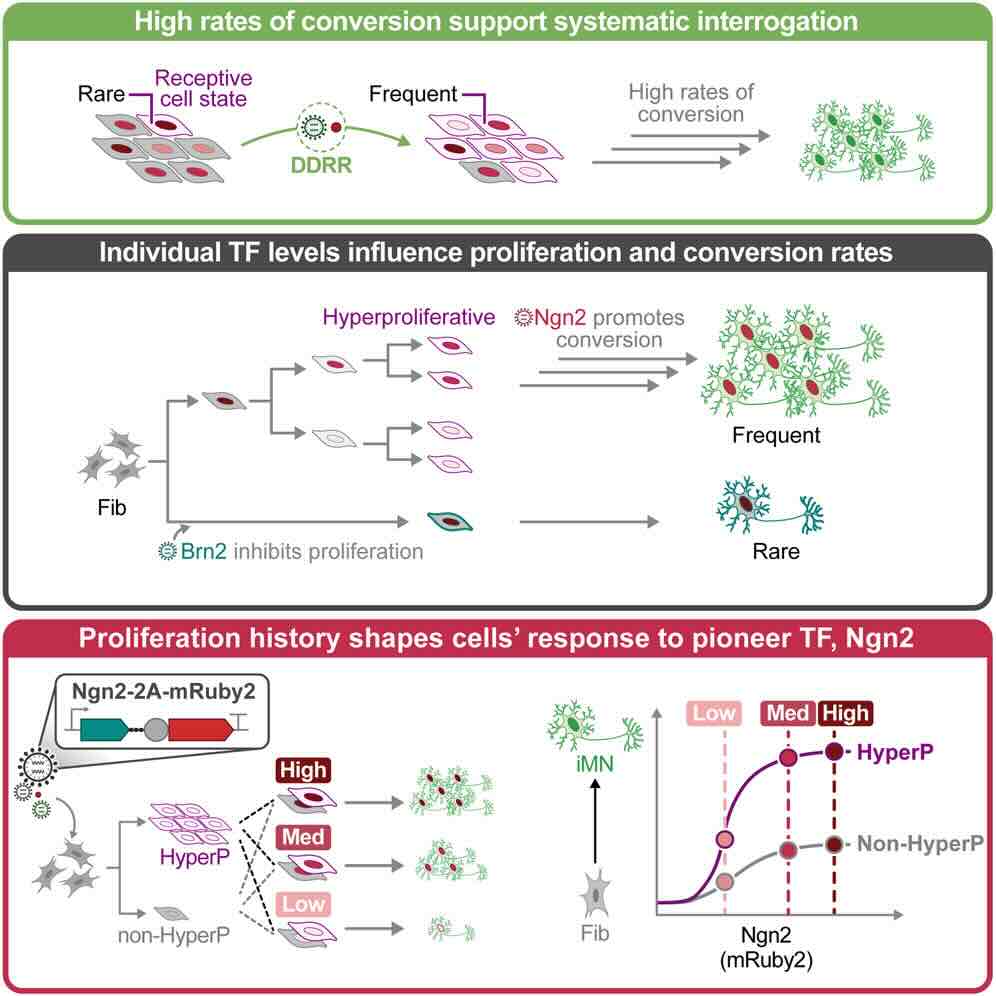
Een opsomming van de vele voordelen van directe omzetting van huidcellen in motorneuronen (volgens de onderzoeksters) (afb: Kate Galloway et al./Cell Systems)
Het omzetten van een type cel in een ander type, bijvoorbeeld een huidcel in een hersencel, was al mogelijk via een proces waarbij de huidcel eerst moet worden geprest een pluripotente stamcel te worden en vervolgens moest die worden gedifferentieerd tot een hersencel. Onderzoeksters van MIT hebben nu een vereenvoudigd proces bedacht dat de stamcelfase omzeilt en een huidcel direct omzet in een hersencel (motorneuron). Dat zou veel sneller zijn dan de ‘oude’ methode en ook een veel hogere opbrengst opleveren. Lees verder

Clive Svendsen met enkele collega’s voor een beeldscherm (afb: Cedars Sinai)
Onderzoekers hebben een gecombineerde stamcel- en gentherapie ontwikkeld die, vooralsnog in theorie, motorneuronen in de hersens of het ruggenmerg kan beschermen tegen afsterving in patiënten met amyotrofe laterale sclerose (ALS). De methode is getest op veiligheid. De werkzaamheid moet nog aan bod komen.
Lees verder

ALS (afb: stichting ALS)

DNA-uitlezing met behulp van CRISPR en nanoporiën (afb: Max Planckinstituut)
Een groot deel van ons genoom bestaat uit herhalingen, wel honderden of duizenden keren. Die herhalingen zijn moeilijk te analyseren. Onderzoekers van het Max Planckinstituut voor moleculaire genetica in Berlijn hebben nu een methode ontwikkeld om dit ‘duistere deel’ van het genoom te kunnen doorzoeken. Die methode is een combinatie van nanoporiegenoomuitlezing en de CRISPR/Cas-methode.
Lees verder

De zenuw- en s[piercellen van ALS-patiënten verschrompelen (afb: www.als.nl)