Aan de universiteit van Toronto heeft een groep onder-zoekers een methode ontwikkeld om de ontwikkeling van stamcellen beter te sturen. “Hierdoor begrijpen we beter hoe we stamcellen kunnen omzetten in klinisch belangrijke celtypen”, zegt promovendus Emanuel Nazareth werkzaam bij het Zandstra-lab van de Canadese universiteit. Lees verder
Tag archieven: pluripotent
Kunnen bloedvatcellen orgaandonatie overbodig maken?

Kunstmatig gekleurde endotheelcellen onder een microscoop. De kern is blauw, het celskelet groen, de actinedraden rood (foto: Wikicommon)
Onderzoekers van het Weill-instituut van de Cornell-universiteit in Ithaca (New York) speculeren over de mogelijkheid dat endotheelcellen (het endotheel is de wand van bloedvaten), ingespoten in de bloedvaten, zieke of beschadigde organen zouden kunnen herstellen. Daarmee zou orgaandonatie op den duur overbodig kunnen worden en zou een einde komen aan de moeizame zoektocht naar orgaandonors. Lees verder
Parkinsonpatiënt heeft misschien baat bij eigen stamcellen

Uit eigen stamcellen ontwikkelden zich gezonde neuronen (links). Niet eigen stamcellen gaven een afweerreactie (rechts) (foto: Cell)
Geïnduceerde pluripotente stamcellen (iPSC) gemaakt van eigen volwassen cellen houden de belofte in dat ze wel eens van grote therapeutische waarde kunnen zijn. Er bestaan echter ook grote twijfels of dat inderdaad zo is. Die eigen stamcellen willen zich nog wel eens ontwikkelen tot kankercellen en dan komt de patiënt natuurlijk van de regen in de drup. Onderzoek met iPS-cellen bij knaagdieren, liet zien dat het eigen afweersysteem die eigen stamcellen aanvallen. Opmerkelijk is dat dat bij primaten niet zo is. Lees verder
Cellen omprogrammeren tot stamcellen wordt een ‘eitje’

Na zes dagen is bijna 100% van de gereprogrammeerde cellen met weinig Mbd3 (rechts) omgezet in stamcellen (geel). Weinig genetisch onveranderde cellen (links) hebben zich omgevormd (rood). (foto: Jacob Hanna, Weizmann-instituut)
Stamcellen zijn een gewild product in de hedendaagse biologie. Voor niet zo heel lang geleden kwamen die van heel vroege embryo’s, waar de celdifferentiatie nog niet was begonnen. Die afkomst heeft altijd een naar bijsmaakje gehouden: er moet een eicel bevrucht worden – in de kern een mensje in wording – om die stamcellen te verkrijgen. Later werden er technieken ontwikkeld om uit volwassen cellen stamcellen te fabriceren. Dat zijn geen alleskunners als de embryonale stamcellen, maar ze konden toch ook wel veel. Dat zijn de pluripotente stamcellen (waarbij pluri staat voor veel en potent voor vermogend oid). Die kun je maken via klonen, maar je kunt ook volwassen cellen reprogrammeren tot stamcellen, als je ze maar de juiste instructies geeft. Het vervelende daarvan, voor de ongeduldige onderzoekers, is dat dat heel lang duurt en tamelijk inefficiënt is. Onderzoekers van het Israëlische Weizmann-instituut zijn er in geslaagd dat proces te versnellen tot een week bij een opbengst van bijna 100%. Lees verder
Stamcellen in muizenlijf ‘gemaakt’
Onderzoekers van het Spaanse kankerinstituut CNIO in Madrid zouden er voor het eerst in geslaagd zijn cellen in levende dieren (muizen) te hebben omgevormd tot stamcellen. Volgens de onderzoekers, onder ‘aanvoering’ van Manuel Serrano, zou dat de mogelijkheid openen om lichamelijke schade, zoals ontstaan door een hartaanval, ter plaatse te ‘repareren’. Helemaal probleemloos is het allemaal niet, want uit hun publicatie in het wetenschapsblad Nature blijkt dat de techniek bij muizen leidt tot het ontstaan van kankercellen. Stamceldeskundigen zijn enthousiast, volgens de BBC, maar stellen ook dat er nog een hoop moet gebeuren vooraleer deze techniek in de praktijk kan worden toegepast.
Stamcellen vormen uit normale lichaamscellen is een techniek die wetenschappers inmiddels onder de knie hebben, maar dat gebeurt in het lab (in vitro). De Spanjaarden zouden het nu voor elkaar gekregen hebben die truc ook in het lichaam van een levend wezen uit te voeren. “Dat is verrassend. Het was niet verwacht. De meesten van ons dachten dat dat niet mogelijk was”, zei Serrano tegen de BBC. De proefdieren waren genetisch zo gemanipuleerd, dat als ze een bepaalde stof (doxycycline) kregen toegediend via hun drinkbakje, bepaalde cellen vier groeifactoren gingen aanmaken die nodig zijn voor het ‘omprogrammeren’ van gewone cellen tot zogeheten geïnduceerde pluripotente stamcellen (iPS). Weefselcellen werden zo dus ’terugveranderd’ in stamcellen. Het vervelende is alleen dat die stamcellen, die kennelijk ‘stuurloos’ waren, zich vervolgens verder ontwikkelden tot kankercellen. Serrano: “Natuurlijk wilden we dit niet. We willen de klok op een beheerste manier terugdraaien. We moeten de voorwaarden zien te vinden om de cellen slechts gedeeltelijk te herprogrammeren zodat ze beschadigd weefsel kunnen repareren.”
Met de gebruikte techniek zou de klok veel verder terug zijn gezet dan met bestaande technieken mogelijk is, met inbegrip van de embryonale stamcellen. Daarom denken sommige stamceldeskundigen ook dat deze techniek niet geschikt is voor therapeutische doeleinden, maar wel de kennis over de ontwikkeling van cellen kan vergroten.
Bron: BBC
Muizenhart klopt weer met mensencellen
 Lei Yang van de universiteit van Pittsburgh
Lei Yang van de universiteit van Pittsburgh
Een onderzoeksgroep rond Lei Yang van de universiteit van Pittsburgh heeft een muizenhart weer aan het kloppen gekregen met menselijke stamcellen. Het resultaat was dus een hybride hart, bestaand uit muizenhartcellen en mensenhartcellen. Het onderzoek moet gezien worden in het streven uitgaande van stamcellen nieuwe organen te maken.
Yang ontdeed een muizenhart van alle cellen. Het overblijvende eiwitgeraamte werd vervolgens ‘herbevolkt’ door hartvoorlopercellen (een voorfase van cellen in de ontwikkeling van stamcel tot hartcel) van mensen. Na een paar weken begon het hart weer te kloppen. De voorlopercellen ontwikkelden zich uit pluripotente stamcellen, die op hun beurt weer waren gekloond van menselijke huidcellen. In een eerdere studie werden menselijke embryocellen gebruikt, maar dat was geen succes. Het is voor het eerst dat een muizenhart geheel ontdaan is van zijn eigen cellen, waarna die vervangen werden door voorlopercellen.
Hoewel het muizenhartje pompte, was het niet sterk genoeg om het bloed effectief rond te pompen. Het bleek dat het hartritme afweek van het ritme van een muizenhart. Er blijft dus nog wel wat werk aan de winkel voor de onderzoekers. Uiteindelijk is het, dus, de bedoeling van Yang en zijn medewerkers om menselijke harten te maken die kunnen worden getransplanteerd. “Met onze methode kunnen we zowel de spier- als bloedvatcellen maken. We hopen gauw menselijk hartweefsel te kunnen maken, maar onze droom is uiteraard een heel menselijk hart.”
Bron: New Scientist
De ideale genreparator ontdekt (?)
Ik vrees dat het nog wel een tijdje zo zal gaan: onderzoeksgroepen die beweren dat ze hét middel of dé methode hebben gevonden. Nu zeggen twee Chinese Amerikanen, Zhonggang Hou van het Amerikaanse Morgridge-instituut en Yang Zhang van de Noordwest-universiteit in het blad van de Amerikaanse academie van wetenschappen (PNAS) dat ze een nieuwe techniek hebben ontwikkeld die veel simpeler dan bestaande technieken ‘foute’ genen zou kunnen repareren. “Hiermee is het mogelijk elk gendefect te herstellen, ook die welke verantwoordelijk zijn voor borstkanker, de ziekte van Parkinson en andere ziekten”, zegt Hou. “Doordat die techniek kan worden toegepast op menselijke pluripotente stamcellen opent die de mogelijkheid voor serieuze therapeuthische toepassingen.”
De onderzoekers maken voor hun ‘genreparator’ gebruik van de bacterie Neisseria meningitidis (veroorzaakt hersenvliesontsteking) als bron voor het eiwit Cas9, dat gebruikt wordt om de defecte genen weg te knippen. Zhang: “We zijn er in geslaagd dit eiwit te sturen met verschillende typen kleine RNA-moleculen, waardoor we in staat zijn heel nauwkeurig genen te verwijderen, te verplaatsen of te repareren. Dat is een stap vooruit in vergelijking met de bestaande technieken als de zinkvingernucleases en TALENs.” Deze technieken maken gebruik van synthetisch gemaakte knipeiwitten. Volgens Hou is het mogelijk met de nieuwe techniek in een paar dagen RNA te synthetiseren, waar dat in de ‘oude’ methoden weken tot maanden zou duren. Volgens James Thompson van het Morgridge-instituut, een van de co-auteurs, maakt deze techniek het mogelijk het hele brede scala aan mogelijkheden van de polypotente stamcel te benutten voor therapeutische doeleinden, maar ook voor het testen van geneesnmiddelen of voor biomedisch onderzoek. De methode zou ook veilig zijn. Andere reparatiemethden zouden nog wel eens last hebben van misknippen (het doorknippen van het DNA-molecuul op een verkeerde plaats). Dat zou bij de deze methode niet het geval zijn. De onderzoekers spreken zelfs van een routinematige labtechniek. Of dat werkelijk werkelijk zo is, zal nog moeten blijken. De praktijk is vaak een harde leermeester.
Bron: EureAlert
Geen stamcellen in beenmerg van muizen gevonden
Onderzoekers van het medisch centrum van de Stanford-universiteit is het niet gelukt embryoachtige stamcellen te vinden in het beenmerg van volwassen muizen. Embryostamcelonderzoek is populair vanwege het vermogen van die cellen zich tot alle typen cellen te ontwikkelen. Het probleem is alleen dat er eerst een bevruchting tot stand moet komen. Dat stuit wereldwijd op grote ethische bezwaren. De pluripotente stamcellen zijn een alternatief, maar die hebben niet de uiterste flexibiliteit die embryonale stamcellen hebben.
In 2006 ontdekten Mariusz Ratajczak en zijn medewerkers dat zich in het beenmerg van muizen en mensen heel kleine pluripotente, embryoachtige cellen zouden bevinden. Later werd dat onderzoeksresultaat steeds meer in twijfel getrokken en werd zelfs aan het bestaan van deze stamcelletjes getwijfeld.
Onderzoekers uit de vakgroep van Irving Weissman, hoogleraar pathologie aan de Stanford-universiteit, hebben geen kleine, pluripotente stamcellen kunnen vinden, ondanks verwoede pogingen de oorspronkelijke experimenten van Ratajczak te reproduceren. Weissman: “We hebben het geprobeerd door de beschreven methoden te herhalen, maar we hebben noch in het bloed noch in het beenmerg van de muizen die cellen aangetroffen”.
De onderzoekers vonden wel dat de kleine deeltjes in het beenmerg van muizen geen cellen waren, maar dode cellen met nog wat DNA. Een andere manier om cellen te identificeren is aan de hand van de sleutelmoleculen op hun oppervlak. Ook dat leverde niks op. Hoewel het oorspronkelijke artikel van Ratajczak beoordeeld was door referenten, hebben andere labs problemen gehad de resultaten te repliceren. Weissman heeft dan ook grote twijfels over het bestaan van de beenmergstamcellen.
Bron: Eurekalert
Ziekte van Down de baas?
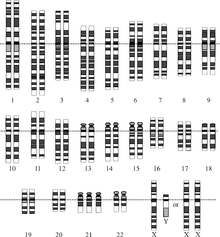
Kunnen we het syndroom van Down de baas? Die ziekte, mensen die daaraan leden werden vroeger ‘mongolen’ genoemd, is terug te voeren tot een extra chromosoom, de 21 in de officiële telling. Onderzoekers rond Jun Jiang van de universiteit van Massachusetts in Worcester (VS) zijn er in geslaagd dat overbodige derde chromosoom uit te schakelen, zo schrijven ze in het wetenschapsblad Nature. Dat betekent overigens niet dat daarmee nu een therapie is tegen deze ziekte. De experimenten zijn uitgevoerd in celculturen in petrischalen. Ze gebruikten voor de uitschakeling een natuurlijke mechanisme dat een van de twee vrouwelijke geslachtshormonen (X-X, waar mannen een X-Y-chromosomenpaar hebben) uitschakelt met behulp van het zogeheten Xist-gen. Dat gen zorgt er voor dat dat tweede X-chromosoom door eiwitten wordt ingekapseld, zodat de genen niet meer kunnen worden afgelezen. De onderzoekers deden hun experimenten met zogeheten pluripotente stamcellen die waren gemaakt uitgaande van huidcellen van een Down-patiënt. Ze voegden het Xist-gen in een kopie van chromosoom-21 toe. Dat overbodige chromosoom werd, zoals gehoopt, vervolgens ingekapseld.
“De afgelopen jaren is er grote voortuitgang gemaakt bij ziektes die door een enkel gen worden veroorzaakt”, zei celbiologe Jeanne Lawrence van de universiteit. “Maar tot nu toe was men er nog niet in geslaagd honderden genen tegelijk uit te schakelen.” Aan de hand van de resultaten van dit onderzoek kan beter bestudeerd worden wat dat derde chromosoom in cellen teweegbrengt. De onderzoekers hopen op den duur een therapie te kunnen ontwikkelen. Daartoe zullen proeven met muizen worden uitgevoerd. In de huidige praktijk worden vruchten die bij prenataal onderzoek het Down-syndroom blijken te hebben veelal geaborteerd.
Bron: Der Spiegel
Menselijke levercellen werken (in muis)
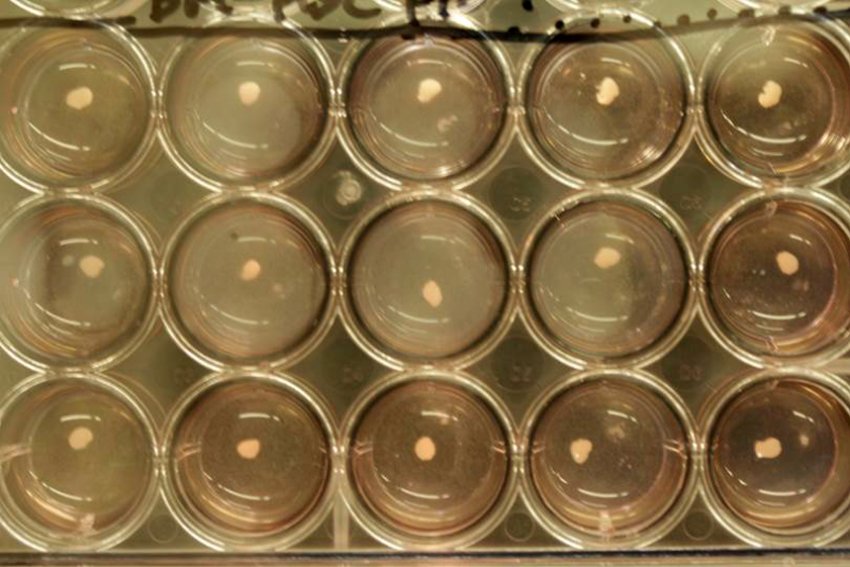 Petrischalen met leverweefsel: een staaltje zelforganisatie van de levercellen (foto Takanori Takebe )
Petrischalen met leverweefsel: een staaltje zelforganisatie van de levercellen (foto Takanori Takebe )
Het is Japanse onderzoekers van de universiteit van stad Yokohama gelukt muizen levercellen te bezorgen, menselijke nog wel. Die cellen functioneerden. De levercellen waren ontwikkeld uit menselijke stamcellen. Na de transplantatie van de cellen duurde het twee dagen voordat de cellen verbonden waren met het celweefsel van de muizen.
Om er achter te komen of de cellen ook echt werkten gaven de onderzoekers de muizen voedsel dat bij mensen anders verwerkt wordt dan bij muizen. In de urine van de dieren werden afvalproducten gevonden die bij de menselijke stofwisseling horen. Ergo, de levercellen werkten in de muizenlevers. De Japanse onderzoekers maakten bij hun experimenten, tot hun eigen verassing, gebruik van het vermogen tot zelforganisatie van cellen.
De hoop bij dit soort onderzoek is gevestigd op het ‘synthetiseren’ van nieuwe organen uit eigen celmateriaal, waardoor er geen afweerreacties van het eigen immuunsysteem optreden. Het zal echter nog wel even duren voor dat het zo ver is. De ontwikkeling is nog lang niet zo ver dat er een ‘volwassen’ orgaan kan worden gemaakt. Zo moet de lever, voor zijn ontgiftende arbeid, verbonden zijn met de gal. Of dat met de door de Japanners gehanteerde methode ook gebeurt, valt nog niet te bezien. Volgens Takanori Takebe van de onderzoeksgroep zal het nog zeker tien jaar duren voor de eerste experimenten met mensen zullen plaatsvinden.
Bijzonder aan het onderzoek is dat de onderzoekers geen gebruik maakten van embryonale stamcellen maar van tot stamcellen omgevormde gewone cellen, de zogeheten pluripotente stamcellen. Rond embryonale stamcellen speelt zich nog steeds een ethische kwestie af, omdat daarvoor in principe eerst embryo’s moeten worden gemaakt. Bij pluripotente cellen speelt die ethische kwestie niet. De Japanners kregen het voor elkaar dat die stamcellen zich ontwikkelden tot levercellen. Aan de kweek in petrischaaltjes (zie foto) werden weefselcellen toegevoegd. Vervolgens leek, tot verbazing van de onderzoekers, alles vanzelf te gaan. De stamcellen organiseerden zich zelf tot orgaanbestanddelen. Tot nu toe ging men er van uit dat dat alleen in de ontwikkeling van een embryo gebeurt.
Bron: Der Spiegel


