 Eierstokken van een fruitvliegje. De eiwitten die een rol spelen in de piRNA-route zijn groen, DNA blauw (foto IMBA)
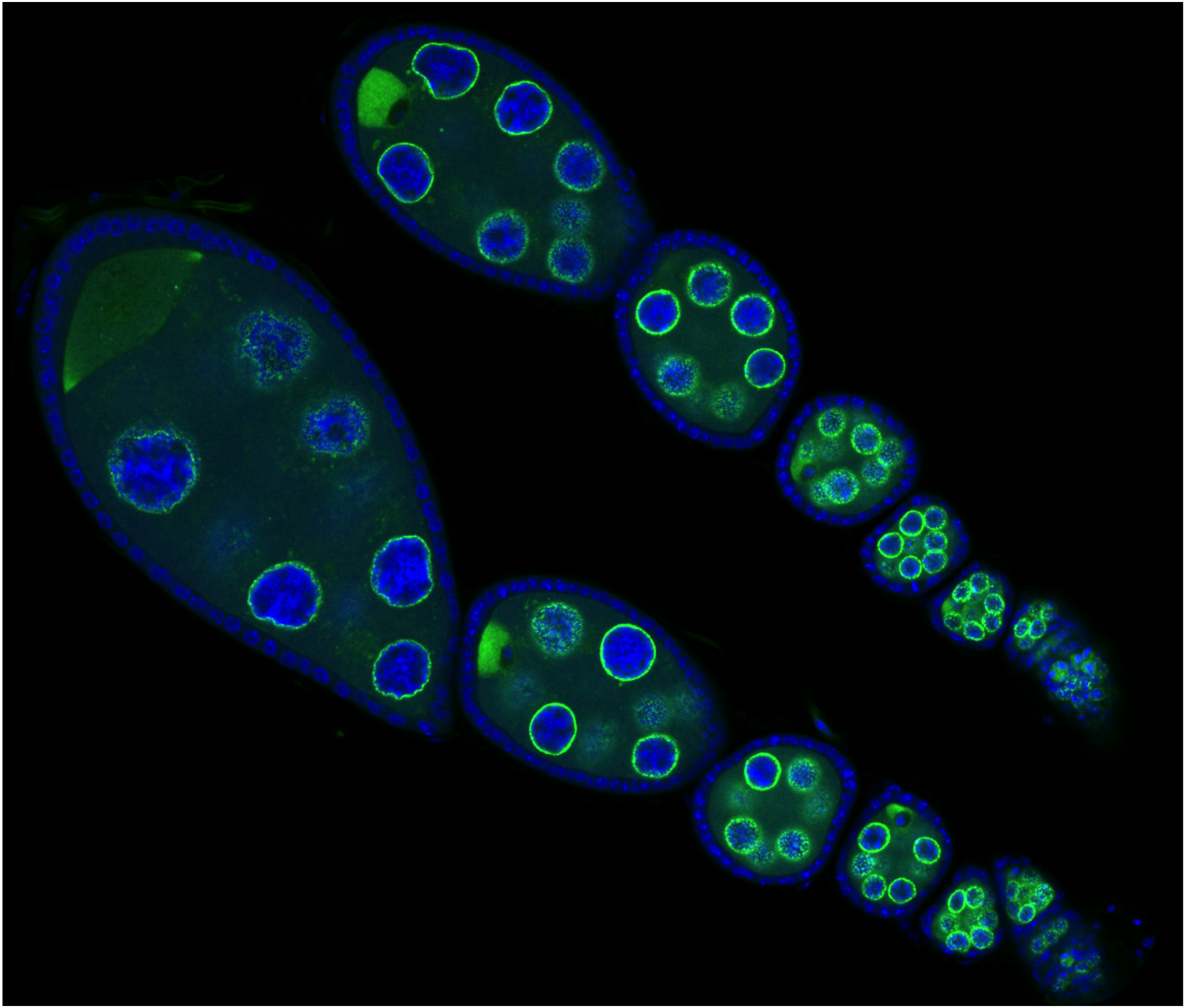
Eierstokken van een fruitvliegje. De eiwitten die een rol spelen in de piRNA-route zijn groen, DNA blauw (foto IMBA)
In de loop van de evolutie is er heel wat ‘ongerief’ in ons DNA terechtgekomen. Springende genen (ook wel transposons genoemd) zijn daar een voorbeeld van. Eigenlijk zouden we die springende genen liever kwijt dan rijk zijn, omdat ze het grote risico in zich bergen van ernstige mutaties en het breken van DNA-strengen. Dat is niet gebeurd. Die transposons worden echter onschadelijk gemaakt door een verdedigingsmechanisme, dat nu door een groep onderzoekers rond Julius Brennecke van het instituut voor moleculaire biotechnologie in Wenen (IMBA) is uitgeplozen bij fruitvliegjes. Het blijkt dat zo’n vijftig genen zijn betrokken bij het belangrijkste beschermingsmechanisme tegen de kwalijke effecten van springende genen, dat aangeduid wordt met piRNA-route.
Pakweg de helft van het menselijke, maar ook ander dierlijke en plantaardige erfgoed (genoom) bestaat uit wat genoemd wordt genoomparasieten zoals transposons. Deze ‘zelfzuchtige’ genen kunnen zich bij de voortplanting min of meer vrij door het DNA-molecuul verplaatsen. Dat is, zoals gezegd, riskant voor de soort, maar planten en dieren hebben zich daartegen gewapend. Je zou het kunnen beschouwen als een soort genoomimmuunsysteem.
Tot nu toe was er weinig van bekend hoe dat mechanisme werkt. Ruw geschetst werkt dat mechanisme met bepaalde eiwitten (Piwi-eiwitten) die binden aan stukjes RNA en zo een complex vormen. Die complexen herkennen transposons en voorkomen dat die stukjes DNA worden omgezet in RNA en verhinderen dus de vorming van ongewenste eiwitten.
De 50 geïdentificeerde genen die bij dat mechanisme zijn betrokken in het fruitvliegje, komen voor een belangrijk deel ook in het menselijk erfgoed voor. De onderzoekers verwachten dan ook dat deze resultaten ook, althans deels, gelden voor andere dieren (ook mensen). Sommige van die genen zijn nodig voor het produceren van piRNA’s, maar andere zijn verantwoordelijk voor de stofwisseling in de mitochondriën (de ‘energiecentrale’ van een cel), het transport van RNA of de transcriptie.
De ontdekking van de Weense onderzoekers is pas het begin. Er blijven genoeg vragen over. Bijvoorbeeld waarom die transposons nog in ons erfgoed zitten. Je zou kunnen zeggen dat dat een ingebouwd mechanisme voor evolutie is, maar is dat ook zo? Een andere kwestie is natuurlijk hoe de piRNA’s van generatie op generatie worden doorgegeven. Wordt, ongetwijfeld, vervolgd.
Bron: AlphaGalileo (foto: IMBA)

 Ons
Ons 
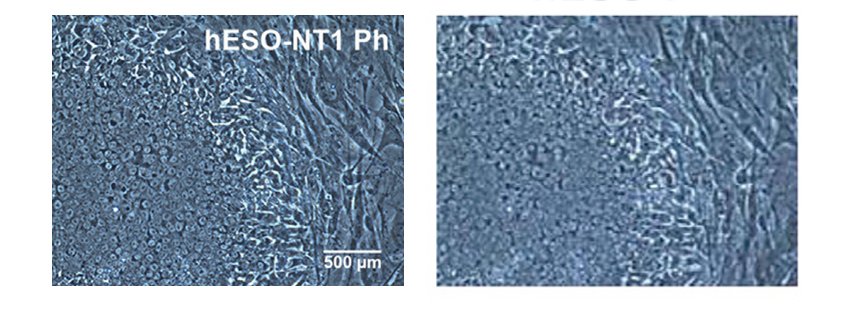 Links de cultuur van stamcellen die via klonen zou zijn ontwikkeld, rechts de op natuurlijke verkregen embryonale stamcellen (foto Der Spiegel).
Links de cultuur van stamcellen die via klonen zou zijn ontwikkeld, rechts de op natuurlijke verkregen embryonale stamcellen (foto Der Spiegel).

 Stamcellen zijn heftig in. Was gister te
Stamcellen zijn heftig in. Was gister te 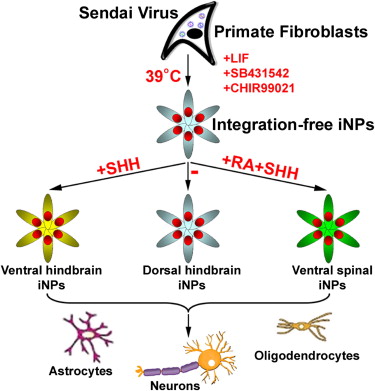 Onderzoekers van de universiteit van Wisconsin hebben bindweefselcellen (fibroblasten) omgetoverd tot
Onderzoekers van de universiteit van Wisconsin hebben bindweefselcellen (fibroblasten) omgetoverd tot 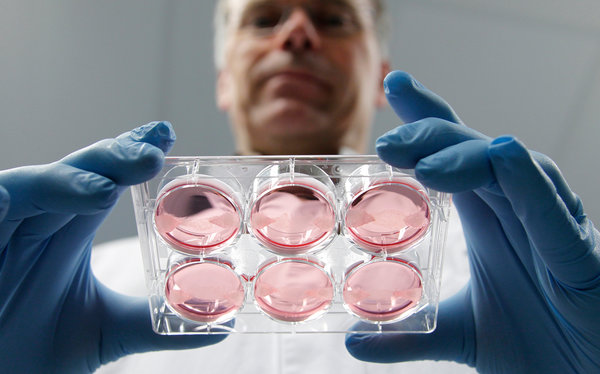 Het klinkt prachtig: spiercellen in een lab maken, waar we dan onze behoefte aan vlees mee kunnen verzadigen, maar de voeten en aarde zitten nog (?) in de weg. Vorig jaar kwam dat nieuwtje naar buiten.
Het klinkt prachtig: spiercellen in een lab maken, waar we dan onze behoefte aan vlees mee kunnen verzadigen, maar de voeten en aarde zitten nog (?) in de weg. Vorig jaar kwam dat nieuwtje naar buiten.