Het komt allemaal steeds dichter bij, die nieuwe, genetisch helemaal ‘opgekalefaterde’ mens. Uit een artikel in FASEB Journal, een blad op het gebied van experimentele biologie, blijkt dat genen die, met behulp van een ‘lam’ virus, ingebracht zijn in zaadcellen ook daadwerkelijk terecht zijn gekomen in het erfgoed van de nakomelingen en ook bij de nakomelingen daar weer van. Dat dat kan is aangetoond bij muizen. ‘Ontwerpzaad’. Lees verder
Categorie archieven: Gentherapie
Leer afweercellen kankercellen te herkennen
Leer immuuncellen kankercellen te herkennen en dat komt alles terecht. In de vele jaren van het wereldwijde kankeronder-zoek zijn al vele voorstellen en ideeën geopperd om die gevreesde ziekte (eigenlijk een conglomeraat van woekerende ziektes) een definitief halt toe te roepen. De Amerikaanse kankeronderzoeker Michel Sadelain van het Memorial Sloan-Ketheringkankercentrum in New York heeft in maart vijf patiënten met bloedkanker (in jargon: acute lymfatische leukemie) behandeld met eigen immuuncellen, die genetisch zo aangepast waren dat ze kankercellen herkenden en, hopelijk, zouden vernietigen. Bij vier was er verbetering opgetreden en bij een patiënt was de leukemie binnen acht dagen helemaal verdwenen. Bemoedigend, noemt Sadelain dat. Hij heeft, zo meldt het populairwetenschappelijk blad New Scientist, nu elf andere patiënten behandeld met een overeenkomstig resultaat. Ook klinische proeven bij andere kankersoorten laten bemoedigende resultaten zien, stelt het blad.
Lees verder
Gentherapie in de maak voor bloederziekte
Het lijkt er op dat een gentherapie lijders aan de bloeder-ziekte kan helpen aan de zo node gemiste stollingsfactor-en. Het bloed van die patiënten stolt moeilijk omdat bepaalde stollingsfactor-en ontbreken en elke bloeding zou fataal kunnen zijn. Amerikaanse onderzoekers hebben daar nu een gentherapie voor ontwikkeld. De reparatie van het defect begint met het in bloedstamcellen inbouwen van het gen dat zorgt voor de aanmaak van de ontbrekende stollingsfactor of -factoren. Vervolgens worden die ‘gerepareerde’ bloedstamcellen bij de patiënt weer ingespoten. Proeven met honden bleken succesvol: tweeeneenhalf jaar na de behandeling hadden de honden nog steeds geen last van de voor bloederlijders typerende heftige bloedingen. Lees verder
Geeft een slapend gen ons het eeuwige leven?
Geeft een slapend gen ons het eeuwige leven? Voor sommigen zou dat mooi zijn, maar ik heb zo mijn twijfels. Onderzoekers van de Harvard-universiteit in Cambridge (VS) denken tenminste dat ze een stap op de weg naar het eeuwige leven hebben gemaakt. Dat slapende gen, aangeduid met Lin28a zou daarbij de sleutel (kunnen) zijn. Dat gen is actief in embryo’s van vele zoogdieren (ook de mens), maar ‘slaapt’ bij volwassenen. Muizen met een geactiveerd Lin28a-gen herstelden veel sneller de schade aan spieren en (bepaalde) weefsels dan muizen met een inactief Lin28a-gen. Ook hun haar groeit sneller. Ook nooit weg. De onderzoekers meldden niet dat de muizen langer leefden.
Lees verder
HIV-eiwit maakt gentherapie wat minder riskant
Gentherapie kan goed uitpakken, maar het kan ook vreselijk fout gaan. Bij gentherapie wordt vaak gebruik gemaakt van het Murine Leukemie-virus (LMV), maar dan ontdaan van zijn DNA; een zogeheten vector. Als het mis gaat dan krijgt de behandelde patiënt leukemie en dat is natuurlijk niet de bedoeling. Onderzoekers van de Katholieke universiteit Leuven hebben de oplossing gevonden in een eiwit van een ander berucht virus: HIV.
Lees verder
De ideale genreparator ontdekt (?)
Ik vrees dat het nog wel een tijdje zo zal gaan: onderzoeksgroepen die beweren dat ze hét middel of dé methode hebben gevonden. Nu zeggen twee Chinese Amerikanen, Zhonggang Hou van het Amerikaanse Morgridge-instituut en Yang Zhang van de Noordwest-universiteit in het blad van de Amerikaanse academie van wetenschappen (PNAS) dat ze een nieuwe techniek hebben ontwikkeld die veel simpeler dan bestaande technieken ‘foute’ genen zou kunnen repareren. “Hiermee is het mogelijk elk gendefect te herstellen, ook die welke verantwoordelijk zijn voor borstkanker, de ziekte van Parkinson en andere ziekten”, zegt Hou. “Doordat die techniek kan worden toegepast op menselijke pluripotente stamcellen opent die de mogelijkheid voor serieuze therapeuthische toepassingen.”
De onderzoekers maken voor hun ‘genreparator’ gebruik van de bacterie Neisseria meningitidis (veroorzaakt hersenvliesontsteking) als bron voor het eiwit Cas9, dat gebruikt wordt om de defecte genen weg te knippen. Zhang: “We zijn er in geslaagd dit eiwit te sturen met verschillende typen kleine RNA-moleculen, waardoor we in staat zijn heel nauwkeurig genen te verwijderen, te verplaatsen of te repareren. Dat is een stap vooruit in vergelijking met de bestaande technieken als de zinkvingernucleases en TALENs.” Deze technieken maken gebruik van synthetisch gemaakte knipeiwitten. Volgens Hou is het mogelijk met de nieuwe techniek in een paar dagen RNA te synthetiseren, waar dat in de ‘oude’ methoden weken tot maanden zou duren. Volgens James Thompson van het Morgridge-instituut, een van de co-auteurs, maakt deze techniek het mogelijk het hele brede scala aan mogelijkheden van de polypotente stamcel te benutten voor therapeutische doeleinden, maar ook voor het testen van geneesnmiddelen of voor biomedisch onderzoek. De methode zou ook veilig zijn. Andere reparatiemethden zouden nog wel eens last hebben van misknippen (het doorknippen van het DNA-molecuul op een verkeerde plaats). Dat zou bij de deze methode niet het geval zijn. De onderzoekers spreken zelfs van een routinematige labtechniek. Of dat werkelijk werkelijk zo is, zal nog moeten blijken. De praktijk is vaak een harde leermeester.
Bron: EureAlert
Ziekte van Down de baas?
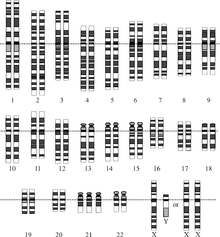
Kunnen we het syndroom van Down de baas? Die ziekte, mensen die daaraan leden werden vroeger ‘mongolen’ genoemd, is terug te voeren tot een extra chromosoom, de 21 in de officiële telling. Onderzoekers rond Jun Jiang van de universiteit van Massachusetts in Worcester (VS) zijn er in geslaagd dat overbodige derde chromosoom uit te schakelen, zo schrijven ze in het wetenschapsblad Nature. Dat betekent overigens niet dat daarmee nu een therapie is tegen deze ziekte. De experimenten zijn uitgevoerd in celculturen in petrischalen. Ze gebruikten voor de uitschakeling een natuurlijke mechanisme dat een van de twee vrouwelijke geslachtshormonen (X-X, waar mannen een X-Y-chromosomenpaar hebben) uitschakelt met behulp van het zogeheten Xist-gen. Dat gen zorgt er voor dat dat tweede X-chromosoom door eiwitten wordt ingekapseld, zodat de genen niet meer kunnen worden afgelezen. De onderzoekers deden hun experimenten met zogeheten pluripotente stamcellen die waren gemaakt uitgaande van huidcellen van een Down-patiënt. Ze voegden het Xist-gen in een kopie van chromosoom-21 toe. Dat overbodige chromosoom werd, zoals gehoopt, vervolgens ingekapseld.
“De afgelopen jaren is er grote voortuitgang gemaakt bij ziektes die door een enkel gen worden veroorzaakt”, zei celbiologe Jeanne Lawrence van de universiteit. “Maar tot nu toe was men er nog niet in geslaagd honderden genen tegelijk uit te schakelen.” Aan de hand van de resultaten van dit onderzoek kan beter bestudeerd worden wat dat derde chromosoom in cellen teweegbrengt. De onderzoekers hopen op den duur een therapie te kunnen ontwikkelen. Daartoe zullen proeven met muizen worden uitgevoerd. In de huidige praktijk worden vruchten die bij prenataal onderzoek het Down-syndroom blijken te hebben veelal geaborteerd.
Bron: Der Spiegel
Succesvolle genmanipulator onder verdenking
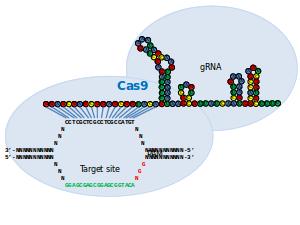
Synthetische biologie staat (en valt) met de vaardigheid het erfgoed te manipuleren (oneerbiedig gezegd: het knippen en plakken van genen). Synthetische eiwitten, zogeheten CRISPR Cas RGN’s, leken daarbij perfect gereedschap. Je kon, bij wijze van spreken, naar believen stukjes DNA op een bepaalde plek in het genoom plakken of het er uit verwijderen. Een truc die bacteriën gebruiken om virussen en andere ziekteverwekkers onschadelijk te maken.
Dat mooie gereedschap blijkt toch zijn kwalijke kantjes te hebben, zo blijkt uit onderzoek van een groep aan het algemeen ziekenhuis in Massachusetts. De plak-en-knip-eiwitten plakten niet alleen stukjes DNA op de beoogde plaatsen, maar ook elders. Dat betekent niet meteen dat dit mooie gereedschap in de vuilnisbak kan worden gegooid. “We zullen”, zei J. Keith Joung van het ziekenhuis, ” de methode moeten verfijnen.”
Het gereedschap bestaat uit een combinatie van instrumenten. Het enzym Cas9, de schaar, is gekoppeld aan een kort stukje RNA dat past op het beoogde stukje DNA. Zoals gezegd is de gentechniek ‘geleend’ van bacteriën. Die kopiëren stukjes genetische codes van virussen of andere indringers en plakken dat in hun eigen DNA. Als dezelfde indringer zich later weer meldt, wordt diens DNA, met behulp van Cas9 in combinatie met het in eigen DNA geplakte stukje genetische code, effectief onschadelijk gemaakt.
Sinds een jaar passen onderzoekers die methode nu toe op het erfgoed van fruitvliegjes, zebravissen, muizen en menselijke cellen. Deze techniek zou een stuk effectiever zijn dan andere technieken die worden gebruikt voor het veranderen van het erfgoed als zinkvingernucleases (ZFN’s) of transcriptie-activatorachtige effectornucleases (TALEN’s). RGN’s kunnen zo worden ‘geprogrammeerd’, dat ze op diverse plaatsen nieuwe stukjes DNA kunnen plakken.
Het ging volgens de onderzoekers niet alleen mis bij stukjes DNA die maar een paar nucleotiden verschillen van het beoogde stukje (dat zou je een ‘vergissing’ kunnen noemen), maar ook bij stukjes DNA die tot wel vijf nucleotiden verschilden van het stukje DNA dat in het genoom geplakt moest worden. Dat misplakken is niet waargenomen bij de andere genmanipulatietechnieken. Joung heeft er alle vertrouwen in dat de problemen met de RGN-techniek kunnen worden opgelost, zodat die ook kan worden gebruikt voor therapeutische doeleinden bij mensen.
Bron: Science Daily (plaatje addgene)
Hooggerechtshof VS verbiedt octrooiering natuurlijke genen
 De Amerikaanse opperrechter Clarence Thomas
De Amerikaanse opperrechter Clarence Thomas
Menselijke genen kunnen niet gepatenteerd worden. Dat heeft het Amerikaanse hooggerechtshof unaniem besloten. Kunstmatig gemaakte stukjes DNA zijn wél octrooieerbaar, stelde het hof. In Amerika was het, in tegenstelling tot Europa, al 30 jaar gebruikelijk om ook stukjes natuurlijk DNA te octrooieren. De zaak ging om patenten van een bedrijf uit Utah (Myriad Genetics, Salt Lake City) op genen die betrekking hadden op borst- en op baarmoederhalskanker. De Amerikaanse biotechnologische sector was zwaar in het geweer gekomen tegen een ban op DNA-patenten. Die zou grote investeringen in genonderzoek en in gentherapieën op losse schroeven zetten. Opperrechter Clarence Thomas betoogde dat een stuk DNA een product van de natuur is en niet patenteerbaar is omdat dat gen toevallig door de patentaanvrager geïsoleerd is.
Bron: BBC
Hart kan nieuwe impuls van virus krijgen
200 patiënten in Europa en Amerika die lijden aan hartfalen zullen via een onschadelijk virus een gen ‘geïmplanteerd’ krijgen dat het beschadigde hart weer goed zou moeten laten functioneren . In een eerder klinische proef is gebleken dat deze gentherapie doet wat die moet doen en niet schadelijk is voor de patiënt. Volgens Alexander Lyon, cardioloog aan het Royal Brompton Hospital en deelnemer in de klinische proef, is het voor het eerst dat gentherapie gebruikt wordt om defecte hartcellen te repareren.
Hartfalen kan het gevolg zijn van tijdelijk zuurstofgebrek bij een hartaanval. Het hart is dan niet goed meer in staat bloed rond te pompen. Voor de patiënt wordt dan bijna elke inspanning te groot.
Onderzoekers van het Imperial College of London ontdekten dat mensen die leden aan hartfalen te weinig van een bepaald eiwit (SERCA aanmaakten. Dat eiwit is verantwoordelijk voor de calcium-kringloop, een element dat wezenlijk is voor de hartslag. Ze ontwikkelden een virus met een gen (SERCA2a) dat het eiwit produceert dat verantwoordelijk is voor de calcium-kringloop. Het virus wordt via een ader in het been van de patiënt in het hart gebracht. Tot nu toe is er geen methode om hartfalen om te keren en moet een patiënt zich zien te redden met medicijnen.
Gentherapie is in wezen een simpele behandelingsmethode, maar door enkele desastreus verlopen klinische proeven is de medische wereld nogal huiverig voor de toepassing van deze techniek. Als de proef slaagt dan is er een methode om hartcellen weer volledig functioneel te maken. Een andere benaderingswijze is het hart de mogelijkheid geven om nieuwe cellen te genereren.
Bronnen: New Scientist, BBC





