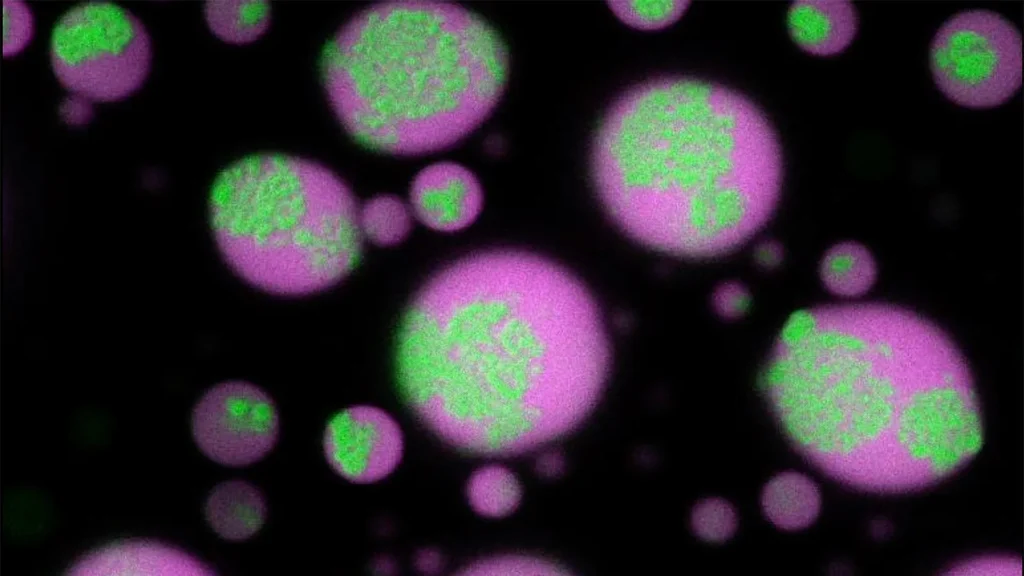
RNA-klonteringen(groen) vallen geleidelijk uiteen in biomoleculaire condensaten (magenta), waardoor het RNA weer oplosbaar wordt. Dit gebeurde nadat een antisense-oligonucleotide, ontwikkeld door het team van Priya Banerjee, aan het condensaat werd toegevoegd. (afb: Universiteit van Buffalo)
Wetenschappers hebben ontdekt hoe bepaalde eiwitklonteringen in de hersens ontstaan en hebben ook een oplossing daarvoor bedacht. en laten ze verdwijnen. Eiwitklonteringen in de hersens komen voor bij de ziektes van Alzheimer, van Parkinson en naar het schijnt (ik=as was me er niet van bewust) ook bij ALS (amyotrofe laterale sclerose) en de ziekte van Huntington.
Bij de laatste twee ziektes gaat het om kleverige RNA-kluwens die kleine vloeistofachtige druppeltjes vormen in cellen en die lang kunnen blijven bestaan, ook nadat hun omgeving is verdwenen. Door introductie van het kleverige eiwit G3BP1, konden de onderzoekers de vorming van de RNA-klonteringen stoppen en met een speciaal ontworpen stukje RNA (ASO, in afko) konden ze die zelfs oplossen. Overigens is het mij niet duidelijk wat de verwijdering van die klonteringen voor de ziek(t)e betekent. Lees verder →