Kort nadat Shoukrat Mitalipov het opzienbarende nieuws via het wetenschapblad Cell had bekend gemaakt dat hij met zijn medewerkers via klonen embryonale stamcellen had ontwikkeld, maakten zelfbenoemde referenten op de webstek PubPeer bekend dat in het Cell-artikel foto’s meermalen zijn gebruikt met een ander bijschrift. Zo zou een en dezelfde foto zijn gebruikt om de gekloonde stamcellen te tonen terwijl dezelfde foto ook de illustratie moest zijn van op conventionele wijze verkregen embryonale stamcellen (namelijk van embryo’s).
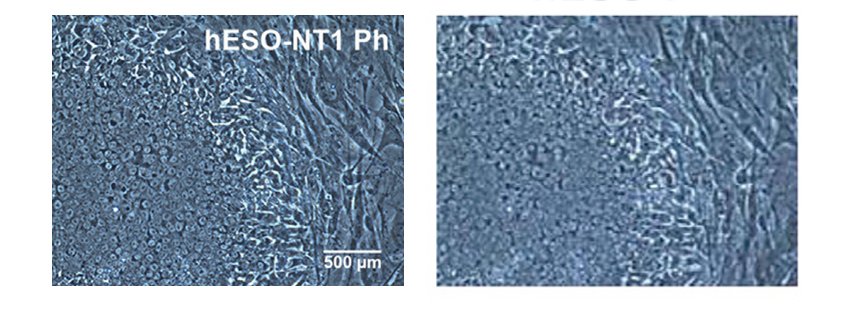 Links de cultuur van stamcellen die via klonen zou zijn ontwikkeld, rechts de op natuurlijke verkregen embryonale stamcellen (foto Der Spiegel).
Links de cultuur van stamcellen die via klonen zou zijn ontwikkeld, rechts de op natuurlijke verkregen embryonale stamcellen (foto Der Spiegel).
De gedachten gaan meteen naar de Zuid-Koreaan Woo Suk Hwang die in 2005 door de mand viel toen hij beweerde via klonen embryonale stamcellen te hebben ontwikkeld. Of dat bij het Mitalipov c.s. ook zo is, valt nu nog niet te zeggen. Verschillende onderzoekers wijzen op de korte tijd die de onderzoekers kregen om het artikel persklaar te maken: 30 april ontvangen, 3 mei gereviseerd en geaccepteerd, 15 mei gepubliceerd. “De resultaten zijn echt, de cellijnen zijn echt, alles is echt”, zei Mitalipov tegen het wetenschapsblad Nature. Ter ontlasting voor de onderzoekers kan gezegd worden dat er niet met de foto’s is geknoeid. Vreemd is natuurlijk wel dat ook de redactie van Cell de gelijkenis niet is opgevallen. Of zou ook die onder extreme tijdsdruk hebben gestaan?
Bronnen: New Scientist, Der Spiegel (foto Der Spiegel)


 Stamcellen zijn heftig in. Was gister te
Stamcellen zijn heftig in. Was gister te  Het klinkt prachtig: spiercellen in een lab maken, waar we dan onze behoefte aan vlees mee kunnen verzadigen, maar de voeten en aarde zitten nog (?) in de weg. Vorig jaar kwam dat nieuwtje naar buiten.
Het klinkt prachtig: spiercellen in een lab maken, waar we dan onze behoefte aan vlees mee kunnen verzadigen, maar de voeten en aarde zitten nog (?) in de weg. Vorig jaar kwam dat nieuwtje naar buiten.  Het hart is een fenomenaal orgaan. Er is waarschijnlijk geen door de mens gemaakte pomp die het beter en, vooral, langer doet. Er is een probleempje: het hart in niet in staat schade te herstellen door het aanmaken van nieuwe hartcellen. Dat blijkt de ‘schuld’ van een enkel gen te zijn aangeduid met
Het hart is een fenomenaal orgaan. Er is waarschijnlijk geen door de mens gemaakte pomp die het beter en, vooral, langer doet. Er is een probleempje: het hart in niet in staat schade te herstellen door het aanmaken van nieuwe hartcellen. Dat blijkt de ‘schuld’ van een enkel gen te zijn aangeduid met