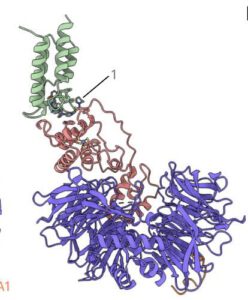
De structuur van SMARCA2 (afb: Georg Winter et al./Nature Chemical Biology
Gerichte afbraak van ziekteverwekkende eiwitten wordt beschouwd als een van de meest veelbelovende strategieën in de modern geneeskunde. In plaats van die alleen te blokkeren, worden ze ook volledig uit de cel verwijderd. Onderzoekers hebben ontdekt dat één enkel molecuul twee onafhankelijke ‘afbraaksystemen’ tegelijkertijd kan activeren. Dit dubbele mechanisme creëert ingebouwde bescherming en zou toekomstige therapieën robuuster en minder vatbaar voor resistentie kunnen maken.
De meeste medicijnen werken door een eiwit te remmen. Ze blokkeren de functie ervan, maar laten het eiwit zelf ongemoeid. Gerichte eiwitafbraak hanteert een andere aanpak: het maakt gebruik van de kwaliteitscontrolemechanismen van de cel om schadelijke eiwitten volledig af te breken. Zogenaamde ‘afbraakmoleculen’ brengen een doeleiwit in de buurt van een E3-ligase (een ‘lijm’eiwit).
Dat enzym markeert het eiwit voor afbraak door het celkringloopsysteem (het proteasoom). De cel gebruikt die brokstukken meestal weer voor de opbouw van nieuwe eiwitten Deze aanpak zou veelbelovend zijn doordat zo ook eiwitten zijn af te breken waarvan de aanmaak moeilijk valt af te remmen. Daarmee wordt niet alleen hun activiteit uitgeschakeld, maar ook hun rol in de cel.
Tot nu toe hadden de meeste van de op dit mechanisme gebaseerde medicijnen echter een nadeel. Ze gebruikten elk slechts één E3-ligase. Als dit proces mislukt – bijvoorbeeld door mutaties of aanpassingen in kankercellen – kan het medicijn ineffectief worden. Het overwinnen van deze kwetsbaarheid is een belangrijke uitdaging in het onderzoek.
In hun recente onderzoek hebben onderzoekers rond Georg Winter bij het CeMM-instituut van de Oostenrijkse academie voor wetenschappenen Alessio Ciulli bij het centrum voor eiwitafbraak CeTPD in Schotland een klein molecuul onderzocht dat zich richt op de SMARCA4/- en -2-eiwitten. Deze eiwitten, als centrale componenten van een chromatinecomplex dat DNA omringt, spelen een cruciale rol in genregulatie en zouden vaak een rol spelen bij kanker.
De onderzoekers ontdekten tot hun verrassing dat het molecuul gebruik maakt van niet één, maar twee verschillende E3-ligasen. Beide routes kunnen onafhankelijk van elkaar de afbraak van het doeleiwit in gang zetten en pas wanneer beide routes zijn gedeactiveerd, stopt het afbraakproces volledig.
Dit principe werkt als een ingebouwd reservesysteem. Als één afbraakroute geblokkeerd raakt, neemt de andere het over. Zo’n ‘achterwacht’ komt veel voor in biologische systemen, maar was tot nu toe zeldzaam in de geneesmiddelenontwikkeling. Het zou een cruciale rol kunnen spelen bij het effectiever maken van geneeswijzen.
Onderzoekers konden met behulp van een combinatie van genetische, biofysische en structurele methoden ophelderen hoe dit systeem werkt. Het molecuul bindt selectief aan het doeleiwit en een E3-ligase, waardoor een zeer specifiek complex ontstaat. Tegelijkertijd kan het ook een tweede ligase aantrekken, waardoor een alternatieve route naar eenzelfde resultaat wordt geopend.
Kleine veranderingen
Door kleine veranderingen aan het molecuul aan te brengen, konden de onderzoekers beïnvloeden welke van de twee ligasen bij voorkeur wordt gebruikt. Minimale genetische verschillen in de ligasen zelf spelen ook een rol, waardoor gerichte controle van de dubbele rekrutering mogelijk is.
“Als een enkel molecuul meer afbraakroutes tegelijkertijd kan activeren, ontstaat er een soort ingebouwde overbodigheid”, zegt Georg Winter. “Dit zou kunnen helpen om een van de grootste problemen met de huidige afbraaktherapieën te overwinnen: hun gevoeligheid voor resistentie.”
Volgens Alessio is dit een belangrijke ontwikkeling. “De structurele details die we hier hebben kunnen verkrijgen zijn opmerkelijk. We kunnen precies zien hoe dat kleine molecuul een nieuwe moleculaire interactie creëert tussen eiwitten die normaal gesproken niet met elkaar in contact zouden komen. Omdat we chemisch kunnen bepalen welk enzym het eigenlijke werk doet, opent dit een nieuwe benadering voor medisch chemici bij de ontwikkeling van de volgende generatie kankermedicijnen.”
De betekenis van deze ontdekking zou verder reiken dan een enkel doeleiwit. Bij kankertherapie ontstaat resistentie vaak doordat cellen manieren vinden om de werkingsmechanismen van geneesmiddelen te omzeilen. Als een geneesmiddel echter meer afbraakroutes tegelijkertijd gebruikt, wordt het voor de kankercel aanzienlijk moeilijker om zich aan te passen.
Bron: idw-online.de
Afbeeldingen in de bijlage
