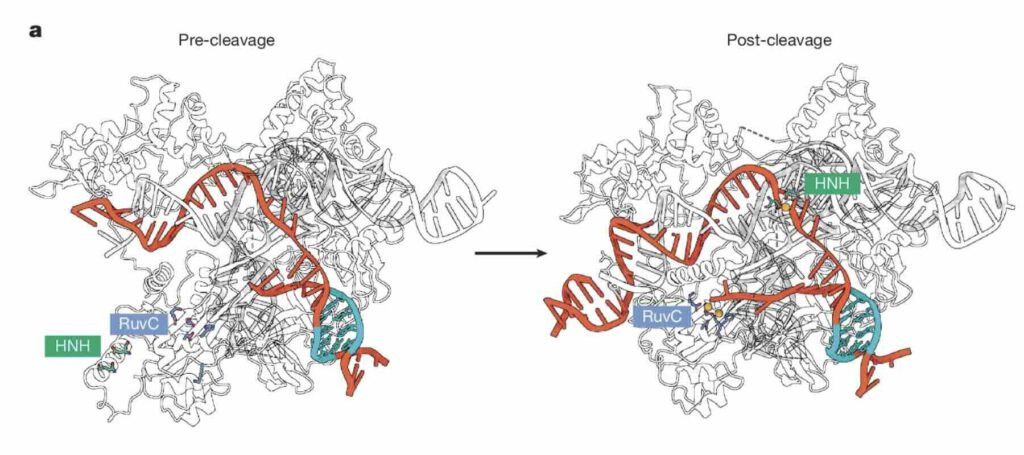
ThermoCas9 voor en na het knippen van DNA (afb: John van der Oost et al./Nature)
Kankercellen zijn meesters in zichzelf verstoppen, maar verraden zich soms door subtiele chemische verschillen met gezonde cellen. Wageningse onderzoekers hebben nu, samen met Amerikaanse collega’s, een manier gevonden om dat verschil uit in methylering van genen uit te buiten om kankercellen te onderscheiden van gezonde cellen. Ze gebruikten daarvoor een pas ontdekte bacteriële CRISPR.
Met een variant van CRISPR, ThermoCas9, slaagden ze erin om tumor-DNA te onderscheiden van gezond DNA op basis van het methyleringspatroon van de genen (die bepaalt welke genen actief zijn en welke niet of minder) en alleen dat eerste te bewerken. De onderzoekers noemen hun werk een veelbelovende stap richting een kankertherapie die kankercellen selectief doodt.
De nieuwe methode draait om methylgroepen, kleine chemische markeringen op het DNA die genen aan- of uitzetten. Deze zogenoemde DNA-methylering zorgt er normaal gesproken voor dat per celtype de juiste genen aan staan. In kankercellen raken die methyleringspatronen verstoord. Precies die onderscheidende moleculaire ‘vingerafdruk’ willen de onderzoekers gebruiken om tumorcellen van gezonde cellen te onderscheiden en aan te vallen.
Voor hun onderzoek gebruikten de wetenschappers ThermoCas9, een CRISPR-variant die ze een aantal jaar geleden in bacteriën ontdekten. Net als andere CRISPR-systemen kunnen onderzoekers deze ThermoCas9 programmeren om specifieke stukjes DNA in een cel op te zoeken en door te knippen met behulp van gids-RNA.
In het lab voegden ze het CRISPR-gereedschap toe aan menselijke cellen in petrischaaltjes: gezonde cellen in het ene schaaltje, tumorcellen in het andere. Ze programmeerden het systeem zo om genen te detecteren die in gezonde cellen gemethyleerd zijn, maar in tumorcellen niet.
Die aanpak werkte zoals gehoopt. ThermoCas9 knipte het DNA in de tumorcellen, maar liet het DNA in gezonde cellen ongemoeid. Het systeem bleek dus in staat om dat kleine chemische verschil tussen gezonde cellen en tumorcellen daadwerkelijk te ‘zienn’ en ernaar te handelen. “Daarmee is deze CRISPR-variant de eerste die reageert op methyleringsverschillen”, zegt John van der Oost. “Dat betekent dat we een systeem in handen hebben dat we gericht naar tumorcellen kunnen sturen.”
Dit onderzoek is het eerste waarin een op CRISPR gebaseerde methode gebruikmaakt van methyleringsverschillen om menselijke kankercellen aan te vallen. “ThermoCas9 gebruikt methylering als een soort adres om kankercellen nauwkeurig aan te vallen, terwijl gezonde cellen onaangetast blijven”, zegt Hong Li van het Van Andelinstituut in Michigan (VS). “Deze bevindingen zouden weleens een doorbraak kunnen zijn.”
Selectief
De verklaring voor dat selectieve gedrag van ThermoCas9 ligt in de manier waarop het knipeiwit zich aan DNA bindt. Voordat een CRISPR-systeem DNA knipt, moet het zich eerst hechten aan een korte herkenningscode naast het doelwit, de zogeheten PAM (Protospacer Adjacent Motif). Bij ThermoCas9 bevat die code een methyleringsplaats, wat betekent dat deze een methylgroep kan bevatten.
Van der Oost: “Het CRISPR-systeem bindt heel nauwkeurig aan die herkenningscode.” Li: “ThermoCas9 is een perfect voorbeeld van de waarde van fundamenteel onderzoek. Je moet weten hoe deze afzonderlijke onderdelen samenwerken,. We hebben met behulp van biochemie en structuurbiologie een mechanisme ontdekt waarvan we hopen dat het op een dag zal leiden tot een nauwkeurigere en effectievere behandeling van kanker.”
Toch is de weg naar een kankerbehandeling nog lang. De huidige studie laat zien dát het systeem selectief kan knippen, maar nog niet dat dit ook voldoende is om tumorcellen te doden. De volgende stap is om het DNA in tumoren zodanig te beschadigen dat de cel sterft. “Dat is een kwestie van essentiële genen verstoren, waardoor de tumorcel niet meer kan functioneren en overleven”, aldus Van der Oost. Voor dat vervolgonderzoek ontvingen hij en postdoc Christian Südfeld eind januari de ERC Proof of Concept-beurs. Daarna moet de therapie nog verder worden getest. “Het zal waarschijnlijk nog minstens tien jaar duren voordat een dergelijke therapie voor patiënten beschikbaar komt”, zegt Van der Oost.
Verder kijken
Intussen kijken de onderzoekers wel al verder dan deze ene toepassing. Ook bij andere ziekten, waaronder kinderkanker (neuroblastoom) en auto-immuunziekten, spelen afwijkende methyleringspatronen een rol. In de toekomst maakt dat ThermoCas9 – of een vergelijkbaar CRISPR-instrument – potentieel breder inzetbaar. Dat zou dan een moleculair gereedschap worden dat zieke cellen herkent aan hun chemische ‘handtekening’ en ze vervolgens gericht uitschakelt. Van der Oosten: “Met die therapie zouden we dan CRISPR gericht naar zieke cellen kunnen sturen om patiënten te behandelen”, speculeert de microbioloog.
Bron: Alpha Galileo
