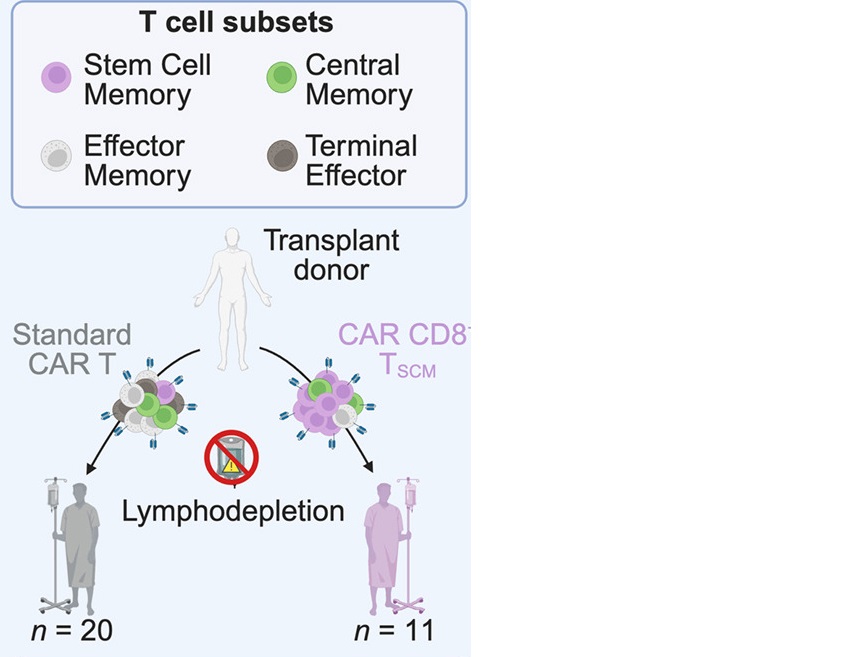
Een bepaald type T-stamcellen zouden kanker met de CAR-T-behandeling geheel doen verdwijnen zonder voorafgaande chemo (afb: Luca Gattinoni et al./Cell)
CAR-T-stamcelgeheugencellen (TSCM’s) zijn zelfvernieuwend, hebben een lange overlevingscapaciteit en kunnen sterke antitumorreacties genereren. Daarom zijn ze veelbelovende kandidaten voor de volgende generatie CAR-T-celtherapieën. Tot nu toe ontbrak bewijs voor hun werkzaamheid bij mensen. Een groep onderzoekers onder leiding van Luca Gattinoni van het Leibnizinstituut voor Immunotherapie (LIT) en James Kochenderfer van het Amerikaanse kankerinstituut meldt nu dat CAR-T-cellen met een TSCM-fenotype veilig en goed verdraagbaar waren in een vroege klinische studie. Bovendien induceerden ze complete tumorregressie bij lage doses, zonder voorafgaande chemo.
De CAR-T-celtherapie heeft vooral succes bij bepaalde bloedkankers. Veel patiënten profiteren echter nog niet permanent van de behandeling, omdat de getransplanteerde CAR-T-cellen vaak onvoldoende delen of niet langdurig in het lichaam aanwezig blijven. Om deze problemen te overwinnen, gebruikten de wetenschappers in hun nieuwe onderzoek T-stamgeheugencellen . Gattinoni en de zijnen ontwikkelden een platformtechnologie voor de productie van dergelijke CAR-gemodificeerde TSCM-cellen voor klinisch gebruik en toonden hun werkzaamheid aan in modellen van acute lymfatische leukemie (ALL).
“De huidige CAR-T-producten kunnen aanzienlijk variëren en deze verscheidenheid komt tot uiting in verschillende behandelingssuccessen en in giftigheid. Daarom hebben we een gestandaardiseerd CD8+-CAR-T-celproduct (een bepaald type T-cel) ontwikkeld met nauwkeurig gedefinieerde eigenschappen, specifiek verrijkt met TSCM-cellen en dat vergeleken met conventionele CAR-T-cellen,” stelt medeonderzoeker Gabriele Inchingolo.
Zoals bleek bij patiënten met een CD19+ B-celziekte na een bloedstamceltransplantatie aantoonde, deelden de CAR-gemodificeerde TSCM-cellen beter en overleefden ze langer dan standaard CAR-T-cellen. Dit resulteerde in complete verdwijning van de tumoren bij lage doses, zelfs zonder de gebruikelijke T-celdodende chemotherapie voorafgaand aan de infusie. Kochenderfer: “De cellen die zijn verkregen met behulp van de TSCM-platformtechnologie leidden tot hogere CAR-T-celniveaus in het bloed van de patiënten en in veel studies zijn hoge CAR-T-celniveaus in het bloed een sterke voorspeller gebleken van klinisch succes.” Gattinoni: “Het feit dat patiënten volledige tumorregressie bereiken met doses van slechts 250 000 cellen/kg, geheel zonder voorafgaande chemotherapie, bevestigt jarenlang voorwerk en opent nieuwe mogelijkheden in het ontwerp van CAR T-cellen.”
Het TSCM-celproduct werd ook goed verdragen. “In deze studie waren er minder gevallen van het vrijkomen van cytokinen dan in de meeste andere CAR-studies waarbij ik betrokken ben geweest”, zegt Kochenderfer. Dat is een veelvoorkomende en potentieel ernstige ontstekingsreactie (cytookinestorm) van het afweersysteem die wordt veroorzaakt wanneer CAR-T-cellen actief worden in het lichaam. Zelfs bij CAR-T-celdoseringen die in de controlegroep tot cytokinestorm leidden, ondervonden patiënten die met TSCM-cellen werden behandeld meestal slechts milde bijwerkingen. Dit suggereert dat het TSCM-product CAR-T-cellen genereert die niet de ernstige bijwerkingen veroorzaken die er anders mee geassocieerd worden.
Constante voorraad
In tegenstelling tot conventionele CAR-T-cellen, die hun stamcelachtige reserves uitputten, behouden CAR-TSCM-cellen een constante voorraad gedurende de gehele therapie, die wordt aangevuld door een geleidelijke uitwisseling van actieve klonen. “De TSCM-cellen worden daarom niet allemaal tegelijk geactiveerd, maar in kleine, opeenvolgende golven. Verschillende klonen worden één voor één actief, zodat het totale reservoir van slapende, stamcelachtige cellen behouden blijft. Voor het eerst zien we dit fundamentele principe rechtstreeks bij mensen,” stelt medeonderzoeker Enrico Lugli.
De onderzoekers konden ook uitvissen waardoor de behandeling bij sommige patiënten niet aansloeg. De oorzaken van het behandelingsfalen lagen minder bij de genmetisch veranderde T-cellen zelf, maar eerder bij externe factoren zoals lage niveaus van het doelwiteiwit (de receptor om kankercellen te herkennen) op de kankercellen, afweeronderdrukkende signalen (met name door interleukine 10) of afweerreacties tegen de CAR-constructen.
Gattinoni: “We hebben aangetoond dat een goed gedefinieerd, stamcelachtig celproduct effectief kan zijn bij lagere doses. Met een homogene TSCM-populatie kunnen we waarschijnlijk een betrouwbaardere afweercel maken, waardoor voorspelbaardere resultaten en gerichtere klinische studies mogelijk worden.” Overigens lijkt er nog wel het een en ander uit te zoeken, alvorens deze behandeling in de klinische praktijk kan worden toegepast.
Bron: idw-oline.de
