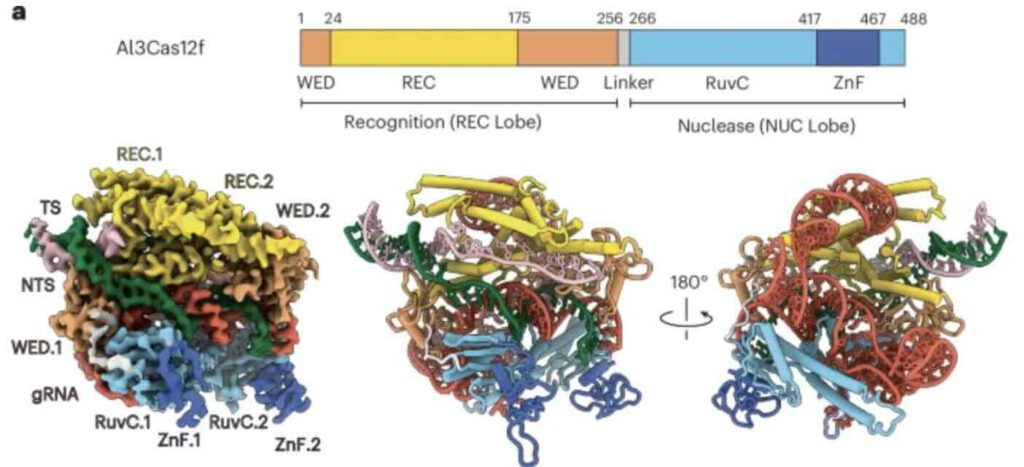
Het compacte ‘knipenzym’ Al3Cas12f zou genoombewerking ‘normaler’ maken (afb: David Taylor et al./Nature Structural & Molecular Biology)
Onderzoekers rond David Taylor van de universiteit van Texas hebben een compacte CRISPR-genbewerkingssysteem ontdekt dat gerichte toediening in het menselijk lichaam mogelijk zou kunnen maken. Ze denken dat dit een belangrijke stap op weg naar een breder klinisch gebruik van deze techniek. Ze kwamen uit bij het natuurlijke knipenzym Al3Cas12f, dat klein genoeg is om te worden vervoerd door (onwerkzaam gemaakt) virussen, een een veelgebruikte techniek om het CRISPR-gereedschap de cellen binnen te loodsen. Vervolgens ontwikkelden ze een verbeterde versie die de genbewerkingsprestaties in menselijke cellen aanzienlijk zou hebben verbeterd.
Deze nieuw ontwikkelde techniek pakt een belangrijke min van de CRISPR-methode aan. De veelgebruikte genbewerkingseiwitten (vaak Cas-en) zijn te groot voor gerichte toedieningssystemen, waardoor klinische toepassingen beperkt blijven tot cellen die buiten het lichaam gemodificeerd worden, zoals bloed en beenmerg.
“Toediening van genbewerkingssystemen is een krachtig middel met brede klinische toepassingen en deze wetenschappelijke ontdekking brengt ons een belangrijke stap dichterbij die toekomst”, zegt Erica Brown, waarnemend directeur van het Amerikaanse instituut van algemene geneeskunde.
De onderzoekers analyseerden de structuur van het enzym met behulp van beeldvormingstechnieken en kunstmatige intelligentie. Ze ontdekten dat het Cas-eiwit een stabieler en hechter complex vormt dan andere enzymen van vergelijkbare grootte, waardoor het effectiever kan functioneren in menselijke cellen.
“De uitgebreide ‘raakvlak’ betekent dat het enzym veel stabieler is. In vergelijking met de andere enzymen die we hebben onderzocht, is Al3Cas12f in principe al voorgeassembleerd en direct klaar voor gebruik nadat de onderdelen zijn geproduceerd”, zegt Taylor, hoogleraar moleculaire biowetenschappen.
De onderzoekers ontwikkelde vervolgens een variant, bekend als Al3Cas12f RKK, die de bewerkingsefficiëntie van het DNA in de cellen aanzienlijk verbeterde van minder dan 10% tot meer dan 80% voor alle geteste doelen. In een veelbewerkt gebied van het genoom bereikte de efficiëntie zelfs 90%. Met andere ‘knipenzymen’ zou die efficiëntie maar een paar procent zijn (zeg ik=as uit het hoofd).
Van de vele varianten die de onderzoekers produceerden, stak Al3Cas12f RKK er met kop en schouders bovenuit. Het team introduceerde de instructies voor RKK rechtstreeks in een lijn van menselijke cellen die oorspronkelijk waren geïsoleerd van een patiënt met leukemie. Mutaties in verschillende van de genen die ze wilden bewerken, werden geassocieerd met ziekten zoals kanker, atherosclerose en amyotrofische laterale sclerose (ALS).
Veelbelovend?
De auteurs verwachten voort te bouwen op hun veelbelovende resultaten. Ze zijn van plan om vervolgens de prestaties van het nuclease (‘knipeiwit’) te testen wanneer het is verpakt in ‘mankgemaakte’ virussen. Als dit succesvol is, zou gentherapie voor veel ziekten een stuk dichterbij de werkelijkheid kunnen komen, denken ze.
Bron: phys.org
