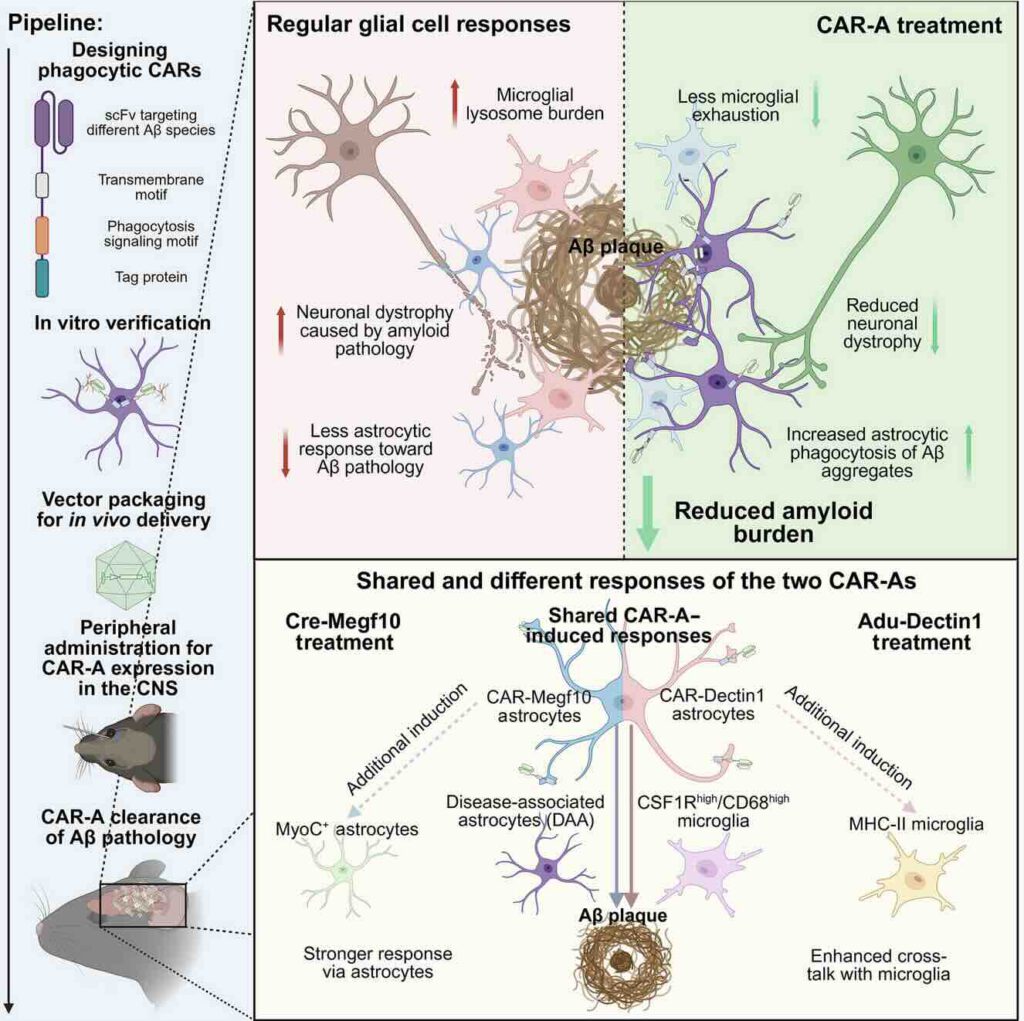
De CAR-A-techniek zou beta-amyloïdeplaques bij muisjes (deels) opruimen. Het gen voor de CA-receptor (=CAR) wordt verpakt in een virusvector in de hersens ingespoten (afb: Marco Colonna et al./Science
Onderzoekers hebben astrocyten (stercellen in de hersens) genetisch zo veranderd dat ze klonteringen van beta-amyloïde opruimen. Dat lijkt een beetje (veel) op de behandeling waarbij T-cellen (een bepaald type afweercellen) genetisch worden geactiveerd om kankercellen te bestrijden in de CAR-T-therapie. Of dat ook betekent dat daarmee de ziekte wordt opgeruimd is nog maar zeer de vraag. Het persbericht meldt niet of de geheugens en cognitieve vaardigheden van de behandelde muisjes ook verbeterden.
De nieuwste klasse medicijnen tegen de ziekte van Alzheimer is de eerste die aantoonbaar de ziekte zelf kan vertragen. Deze behandelingen stellen patiënten doorgaans in staat om ongeveer tien maanden langer zelfstandig te blijven. De medicijnen, bekend als monoklonale antilichamen, werken door de hoeveelheid amyloïde te verlagen, een schadelijk eiwit dat zich in de hersenen ophoopt. Patiënten moeten echter één of twee keer per maand grote doses via infusen toegediend krijgen. Dat is nogal belastend.
Wetenschappers onderzoeken nu manieren om de behandeling minder frequent en mogelijk effectiever te maken. Nu is aan de universiteit van Washington in St. Louis een immuuntherapie ontwikkeld die slechts één injectie vereist. Bij muisjes voorkwam de behandeling de vorming van amyloïdeplaques als die werd toegediend voordat de plaquevorming begon. Toen de behandeling werd gegeven aan muisjes die al plaques hadden, verminderde het de hoeveelheid amyloïde in de hersenen met ongeveer de helft.
De nieuwe strategie is geïnspireerd op CAR-T-celtherapieën die worden gebruikt bij de behandeling van kanker. Bij die therapieën worden T-cellen genetisch veranderd om kankercellen te herkennen en aan te vallen.
In deze Alzheimer-aanpak hebben wetenschappers stercellen, een veelvoorkomend type hersencel dat normaal zorgt voor een gezonde omgeving voor neuronen, uitgerust met een CAR-herkenningsmechanisme waarmee de cellen zich aan specifieke doelen kunnen hechten en deze kunnen vernietigen. Deze CAR-astrocyten (CAR-A) fungeren als krachtige plaquereinigers in de hersens.
“Deze studie markeert de eerste succesvolle poging om astrocyten te modificeren om specifiek beta-amyloïdeplaques in de hersenen van muizen met de ziekte van Alzheimer op te sporen en te verwijderen”, zegt hoofdauteur Marco Colonna. “Hoewel er nog meer onderzoek nodig is om de aanpak te optimaliseren en mogelijke bijwerkingen aan te pakken, bieden deze resultaten een veelbelovende nieuwe mogelijkheid om CAR-astrocyten te ontwikkelen tot een therapie voor neurodegeneratieve ziekten en zelfs hersentumoren.”
De ziekte van Alzheimer begint wanneer een kleverig eiwit, beta-amyloïde genaamd, zich in de hersenen ophoopt en plaques vormt. Deze afzettingen veroorzaken een reeks schadelijke veranderingen die uiteindelijk leiden tot hersenkrimp en een afname van de cognitieve functies.
Normaal gesproken helpen afweercellen in de hersens, microglia genaamd, die troep op te ruimen. Bij neurodegeneratieve ziekten zoals Alzheimer kunnen deze cellen echter overbelast raken en hun vermogen verliezen om de hersenen vrij te houden van dit schadelijke materiaal.
De onderzoekers veranderen astrocyten genetisch tot gespecialiseerde cellen voor het opruimen van amyloïdeplaques. Daartoe introduceerden ze een gen dat een chimere antigeenreceptor (CAR) produceert in astrocyten dat via een kreupel gemaakt virus in de stercellen aan het DNA werd toegevoegd. Het genmateriaal werd via een inenting toegediend. Eenmaal tot expressie gebracht op het oppervlak van de astrocyten, stelde de receptor de cellen in staat bèta-amyloïde-eiwitten op te ruimen.
Muisjes met genetische mutaties die een verhoogd risico op de ziekte van Alzheimer geven, beginnen rond de leeftijd van zes maanden de plaques te ontwikkelen die de hersenen vervuilen. De onderzoekers probeerden de therapie uit op twee groepen van deze Alzheimermuisjes. De eerste groep kreeg het virus met het CAR-gen voordat er plaques verschenen, terwijl de tweede groep de behandeling kreeg nadat hun hersenen al vol zaten met plaques. De onderzoekers wachtten vervolgens drie maanden om de resultaten te evalueren.
Resultaat
Bij de jongere muisjes stopten de gemodificeerde CAR-astrocyten de vorming van plaques. Op een leeftijd van bijna zes maanden, wanneer de onbehandelde diertjes normaal gesproken hersenen vol amyloïdeplaques hebben, vertoonden de behandelde muisjes geen detecteerbare plaques.
Bij oudere muisjes die aan het begin van de behandeling al hersenen vol plaques hadden, verminderde de therapie de hoeveelheid amyloïdeplaques met ongeveer 50% in vergelijking met muizen die een virus zonder het CAR-gen hadden gekregen.
“Net als bij behandelingen met antilichamen is deze nieuwe CAR-astrocyten-immunotherapie effectiever wanneer deze in een vroeg stadium van de ziekte wordt toegediend”, zegt medeauteur David Holtzman, “Het verschil is echter de enkele injectie die de hoeveelheid schadelijke eiwitten in de hersenen van muizen succesvol verminderde.”
Het onderzoeksteam is van plan de CAR-astrocytentherapie verder te verfijnen. Toekomstig onderzoek zal zich richten op het verbeteren van de precisie waarmee de cellen schadelijke eiwitten targeten, zonder de normale hersencelactiviteit te verstoren. De onderzoekers geloven ook dat de technologie kan worden aangepast voor andere ziekten, zoals hersentumoren.
De grote vraag is (en blijft) natuurlijk of deze behandeling de ziekte ook daadwerkelijk bestrijdt. Al meermalen is gebleken dat Alzheimer en de plaques bij elkaar horen, maar dat hersens met beta-amyloïdeplaques niet per se verworden tot Alzheimerhersens. Bovendien lijkt het er op dat die genetisch veranderde stercellen niet alle troep opruimen. Het lijkt er op dat de onderzoekers de hersenfuncties van de behandelde muisjes niet hebben getest (de tekst is voor mij=as niet te lezen).
Bron: Science Daily
