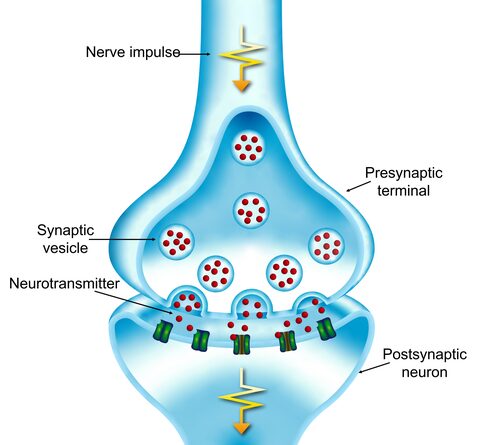
De signaaloverdracht via synapsen van buurcellen in de hersens (afb: OIST)
Het eiwit-eiwitcomplex, bekend uit eerdere onderzoek, bestaat uit de NMDA-receptor en het TRPM4-ionkanaal. NMDA-receptoren zijn betrokken bij de signaaloverdracht tussen zenuwcellen en bevinden zich op het celoppervlak. Ze zijn zowel in de synapsen als buiten deze contactpunten tussen zenuwcellen aanwezig. Die worden geactiveerd door een biochemische boodschapper, de neurotransmitter glutamaat.
Hoewel de activering van synaptische NMDA-receptoren in de hersenen cruciaal is voor het voortbestaan van zenuwcellen en het behoud van cognitieve vermogens, geeft TRPM4 de extrasynaptische NMDA-receptoren toxische eigenschappen. Samen vormen ze een ‘doodscomplex’ dat kan leiden tot zowel schade als de dood van zenuwcellen, legt Hilmar Bading van het Instituut voor Neurobiologie van de universiteit van Heidelberg uit.
Het neurotoxische NMDAR/TRPM4-complex is in veel hogere concentraties aanwezig bij muisjes met een vorm van de ziekte van Alzheimer dan bij gezonde diertjes, zo blijkt uit het onderzoek. Met behulp van de nieuwe farmaceutische verbinding FP802, een zogenaamde ‘TwinFraakvlakremmer’, ontdekt in eerdere studies van Bading en collega’s van het IZN, toonden de onderzoekers aan dat het NMDAR/TRPM4-complex een sleutelrol speelt in de progressie van cognitieve achteruitgang.
In experimenten met muisjes slaagden ze erin het dodelijke eiwit-eiwitcomplex te verbreken met behulp van dit neuroprotectieve molecuul. FP802 bindt zich aan het zogenaamde “TwinF”-raakvlak waardoor TRPM4 interageert met NMDA-receptoren, waardoor de fysieke interactie tussen de twee eiwitten wordt geblokkeerd en het complex oplost.
Vertraagd
“Bij Alzheimermuizen die met het molecuul werden behandeld, werd de ziekteprogressie aanzienlijk vertraagd”, stelt medeonderzoeker Jing Yan. Typische celveranderingen als gevolg van de ziekte van Alzheimer – waaronder het verlies van synapsen en structurele en functionele schade aan mitochondriën – ontwikkelden zich slechts in beperkte mate of helemaal niet, melden de wetenschappers. Cognitieve vaardigheden zoals leren en geheugen bleven grotendeels behouden. Bovendien was de karakteristieke vorming van bèta-amyloïde-afzettingen in de hersenen aanzienlijk verminderd.
Volgens Bading verschilt deze aanpak fundamenteel van eerdere behandelingsstrategieën voor de ziekte van Alzheimer. “In plaats van ons te richten op de vorming of verwijdering van amyloïde uit de hersenen, blokkeren we een stroomafwaarts cellulair mechanisme, het NMDAR/TRPM4-complex, dat de dood van zenuwcellen kan veroorzaken en – in een ziektebevorderende terugkoppelingslus – de vorming van amyloïde-afzettingen bevordert.”.
In eerdere studies kon het team vergelijkbare neuroprotectieve effecten van FP802 aantonen in ziektemodellen voor amyotrofische laterale sclerose (ALS), waarbij het NMDAR/TRPM4-complex ook een rol speelt.
De onderzoekers denken daarom in de nieuwe remmer een potentieel breed toepasbaar farmacologisch principe te hebben gevonden dat de progressie van neurodegeneratieve ziekten zoals Alzheimer en ALS zou kunnen vertragen of zelfs stoppen. Bading stelt echter dat een mogelijke klinische toepassing nog ver weg is. “De eerdere resultaten zijn veelbelovend in de preklinische context, maar uitgebreide farmacologische ontwikkeling, toxicologische experimenten en klinische studies zijn nodig om een mogelijke toepassing bij mensen te verwezenlijken.”
Bron: Alpha Galileo
