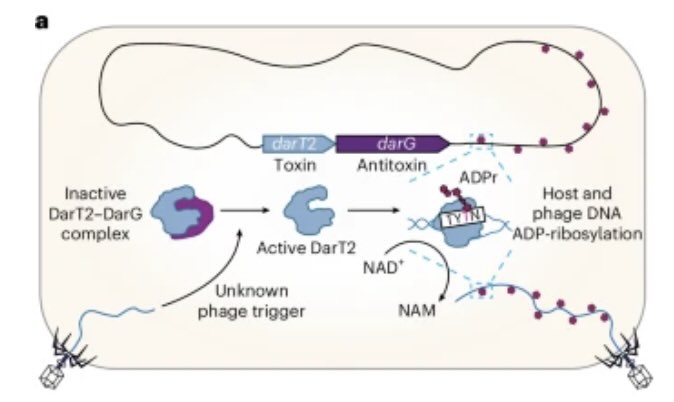
DarT2 zorgt dat het genmateriaal van fagen niet wordt gekopieerd. Als de dreiging voorbij is heft DarG dat weer op. NAM staat voor niacinamide (afb: Chase Beisel et al./Nature Bioltechnology)
Onderzoekers van het Helmholtz Instituut voor RNA-gebaseerd Infectieonderzoek (HIRI) en collega’s hebben een methode ontwikkeld voor het verfijnen van bewerken van genetisch materiaal. Dit omvat het gericht toevoegen van chemische ‘vlaggen’ aan het genoom, wat nieuwe mogelijkheden biedt voor genoombewerking in de geneeskunde, landbouw en biotechnologie.
De gerichte bewerking van genetische informatie heeft de afgelopen jaren enorme voortgang geboekt. Technologieën zoals de CRISPR-Cas9-genschaar en basebewerking – een methode die selectieve veranderingen in DNA mogelijk maakt zonder erin te knippen – zijn al enige jaren ingeburgerd in de wetenschap en klinisch onderzoek. Die hebben de potentie om genetische ziekten te behandelen, planten resistenter te maken tegen plagen of bacteriën te optimaliseren voor biotechnologische doeleinden.
Onderzoekers van het Helmholtzinstituut hebben in samenwerking met de Julius-Maximiliansuniversiteit Würzburg (JMU), samen met wetenschappers van de de universiteit van Noord-Carolina en ETH in Zürich een nieuwe methode ontwikkeld voor precieze DNA-verandering. Hun doel was om het genetische materiaal van bacteriën, planten en menselijke cellen nog preciezer te kunnen veranderen.
Ze werden (alweer) geïnspireerd door een geavanceerd afweersysteem van bacteriën. Deze bacteriën concurreren voortdurend met hun virussen – zogenaamde bacteriofagen. Wanneer fagen bacteriën proberen te infecteren, vertrouwen bacteriën op geavanceerde afweermechanismen, bijvoorbeeld door gebruik te maken van twee enzymen: DarT2 en DarG. DarT2 hecht specifiek een chemische ‘vlag’ aan DNA, waardoor de replicatie ervan wordt geblokkeerd en de aanmaak van het faag-DNA of -RNA wordt gestaakt. Wanneer de dreiging niet langer aanwezig is, deactiveert DarG DarT2 en verwijdert de ‘vlag’. Dit nauwkeurig afgestelde mechanisme voorkomt de verspreiding van het virus en dient nu als basis voor een nieuwe aanpak van genoombewerking.
De wetenschappers noemden deze vorm van modificatie ‘aanhangbewerking’. “Dit stelt ons voor het eerst in staat om volledig nieuwe soorten genetische modificaties te verwezenlijken die met eerdere methoden niet mogelijk waren”, stellen de onderzoekers.
Stel je DNA voor als een notitieboekje, waarbij elke pagina bestaat uit een lange reeks letters. Terwijl conventionele genbewerkingsmethoden meestal individuele letters uit deze reeks verwijderen of vervangen, voegt aanhangbewerking specifiek een chemische groep toe, het ADP-ribosemolecuul, vergelijkbaar met een ‘memo’ dat op een specifieke letter wordt geplakt. De chemische ‘vlag’ zorgt ervoor dat de cel het DNA met hoge precisie modificeert. Welke bewerking hangt echter af van het organisme waarin die vlag wordt gebruikt.
Afhankelijk van organisme
In tegenstelling tot eerdere technologieën, waarbij dezelfde middelen tot vergelijkbare resultaten leidden in alle organismen, waren de effecten van aanhangbewerking zeer verschillend bij bacteriën en eukaryoten zoals schimmels, planten en menselijke cellen. “We zagen dat die methode bij bacteriën leidde tot uitgebreide veranderingen in het genoom op basis van een toegevoegd sjabloon, terwijl in eukaryotische cellen de identiteit van de gemodificeerde DNA-base veranderde”, legt Chase Beisel uit.
“Het feit dat de uitkomst van DNA-reparatie tot zeer verschillende resultaten kan leiden in verschillende organismen, was een van de meest verrassende bevindingen van onze studie”, voegt Constantinos Patinios, voormalig postdoctoraal onderzoeker in het laboratorium van Beisel, toe.
De onderzoekers denken met de nieuwe bacterietechniek talloze nieuwe toepassingen te kunnen realiseren. “Dit breidt de gereedschapskist van genoomonderzoek enorm uit en opent nieuwe deuren voor precisiebiotechnologie en de ontwikkeling van medische therapieën”, legt weer een andere medeonderzoeker, Darshana Guptat, uit. Microben zouden specifiek gemodificeerd kunnen worden, bijvoorbeeld om natuurlijke, gezondheidsbevorderende bacteriën in het menselijk lichaam te optimaliseren of om ziekteverwekkers beter te onderzoeken. In menselijke cellen zou puntbewerking in de toekomst ook kunnen helpen om erfelijke ziekten nauwkeurig te corrigeren en DNA-herstelprocessen in cellen te begrijpen.
“DarT2 is slechts één voorbeeld van het gebruik van bacteriële afweermechanismen in genoomonderzoek”, aldus Harris Bassett, die zijn promotie afrondt in het laboratorium van Beisel. Met andere woorden: er zit nog veel meer in het vat.
Bron: idw-online.de
