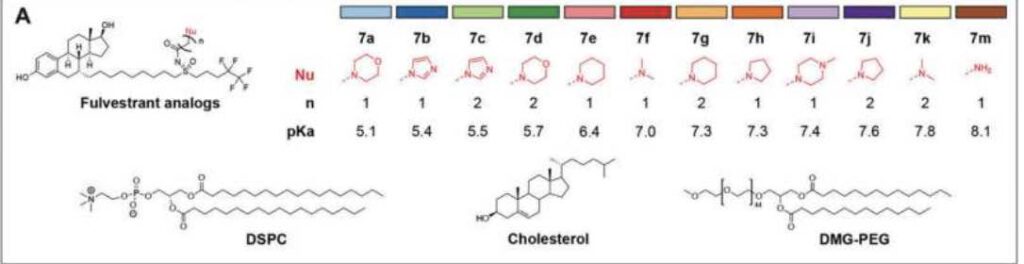
De fulvestrantachtige verbindingen die de onderzoeksters in combinatie met siRNA gebruikt hebben (afb: Molly Shoichet et al./Advanced Materials)
SiRNA is goed gereedschap, alleen nu nog een goede bezorger, meldde ik in dit blog een paar jaar geleden. Mogelijk dat onderzoeksters onder leiding van Molly Shoichet van de universiteit van Toronto die goede bezorger gevonden hebben in de ioniseerbare stoffen die ze met de riRNA’s meestuurden om de korte kernzuren op de gewenste plaats in de cellen te krijgen.SiRNA staat voor klein interfererend RNA. Zo’n RNA-streng bestaat uit zo’n 20 tot 25 bouwstenen van de kernzuren, de nucleotiden.
SiRNA beïnvloedt de genactiviteit. Om dat voor elkaar te krijgen moeten die biomoleculen in de celkern terechtkomen en dat lijkt nogal lastig te zijn. Deels komt dat doordat het enkelstrengige siRNA’s nogal gauw weer uit elkaar wordt ‘getrokken’ door enzymen.
De onderzoeksters wilde een specifiek siRNA in de celkern krijgen. Dat lukte samen met ioniseerbare moleculen. “Dit kan grote veranderingen teweegbrengen om complexe aandoeningen te behandelen, waarbij verschillende signaalroutes moeten worden aangesproken zoals kanker of virusbesmettingen”, zegt medeonderzoeker Kai Slaughter.
Cellen ruimen ‘rommel’, zoals deze indringers, meestal op in endosomen (celblaasjes) en dat is niet de bedoeling. Recent onderzoek met ioniseerbare lipiden (vetachtige stoffen) hadden al een beter resultaat opgeleverd, maar die bleven door de gebruikte nanotechnologie toch achter bij de verwachtingen waardoor niet voldoende intact siRNA in de kern kon worden afgeleverd.
Combinatie
De combinatie van stoffen die makkelijk ionen vormen (in afhankelijkheid van de zuurgraad) en de siRNA’s bleek de kleine interfererende RNA’s wel in voldoende mate in de celkern (die een eigen membraan heeft) te krijgen en kennelijk zijn die ‘medestanders’ nu ook weer ioniseerbare lipides (fulvestrantachtige verbindingen, om wat preciezer te zijn; fulvestrant is een anti-oestrogeen).
De onderzoeksters ontdekten dat fosfolipiden een diepgaande invloed hebben op de endocytose (‘vuilopruiming’) in kankercellen, die werd verbeterd door de nanodeeltjes. Cholesterol is cruciaal voor siRNA-inkapseling. Twee fulvestrant-analogen leverden siRNA af dat de expressie van een reporter-gen in kankercellen aanzienlijk verminderde.
Verdere optimalisatie van de fosfolipide en de formuleringsbuffer leidde tot een groter effect en uiteindelijk uitschakeling van het therapeutisch relevante cycline-E1-gen in medicijnresistente borstkankercellen.
Deze strategie is, schrijven de onderzoeksters, waarschijnlijk breed toepasbaar op een reeks ioniseerbare geneesmiddelen en maakt de toediening van hoge doses van zowel geneesmiddelen als RNA-therapeutica met ruimtelijke en tijdsturing in cellen mogelijk. Uiteindelijk zou deze technologie synergetische behandelingen mogelijk moeten maken die nu nog niet mogelijk zijn. Ik(=as) ben benieuwd.
Bron: phys.org
