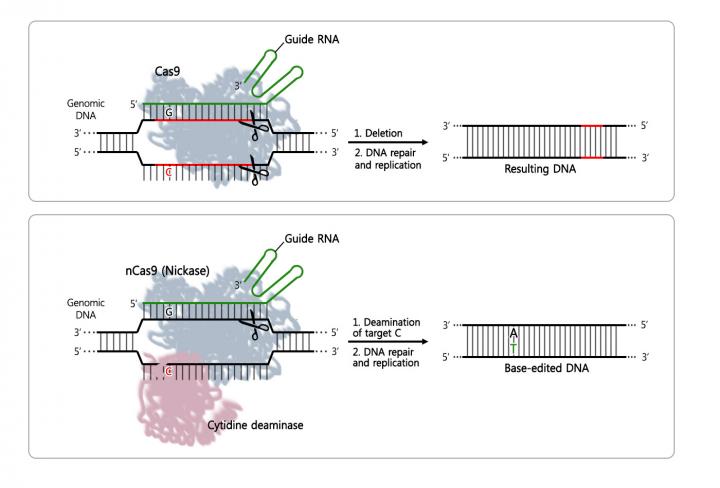
Hier een variant van de genschaar Cas9, nCas9, die slechts een DNA-streng doorknipt in plaats van twee. Daarmee kunnen afzonderlijk basen vervangen worden
Waarschijnlijk is de ontdekking en ingebruikneming van het bacteriële systeem om het genoom te bewerken, CRISPR, een van de belangrijkste wetenschappelijke ontwikkelingen van, op zijn minst, de laatste tien jaar. Onderzoek op het gebied van biologie en geneeskunde zijn sinds een paar jaar ingrijpend veranderd door de komst van die methode. Daarvoor waren er als zinkvingers en TALEN , maar die genoombewerkingsmethoden vallen in het niet bij CRISPR. Die methode geeft hoop op, onder meer, genezing van ernstige ziektes maar houdt ook de dreiging in van kinderen-op-maat en mensverbetering.
Ik heb het in dit blog vaak over CRISPR, veelal in combinatie met Cas9 hoewel dat geen twee-eenheid is , maar hoe het werkt moest je uit de plaatjes en de koppelingen opmaken. Nu een korte uitleg zoals die gepresenteerd is door het Amerikaanse webblad Wired.
Om te beginnen is CRISPR geen enzym of de naam voor een of ander biomolecuul. CRISPR is de Engelse afko voor gegroepeerde regelmatige palindroomherhalingen, die onderdeel vormen van de bacteriële afweer tegen virussen.
Virussen zijn organismen die niet in staat zijn hun eigen DNA te vermenigvuldigen en daarvoor het DNA van hun gastheren gebruiken, zoals bacteriën. Die ontwikkelden daar een beschermingsmechanisme tegen. Er werden eiwitten geproduceerd die het DNA van de aanvallers in stukken knippen. Als de bacterie die aanval overleeft, dan plakt hijzij stukjes van dat virus-DNA in het eigen DNA om het in de toekomst sneller te kunnen herkennen. Dat lijkt heel erg veel op het ‘leervermogen’ van ons eigen afweersysteem. Om die vreemde stukjes DNA af te bakenen werd elk stukje virus-DNA van het eigen DNA gescheiden door die herhaalde, palindroomsequenties. Die stukjes zijn van links naar rechts gelijk aan van rechts naar links, vandaar de term palindroom (zoals neven, parterretrap, paap). Op die manier ontstonden er geen (DNA-)misverstanden.
De volgende keer dat een bekend virus de aanval waagt, kan met meer geweld worden teruggeslagen door de bacterie. Daartoe gebruikt die een groot eiwit, Cas9, dat dient als schaar, die met een kopie van het stukje viruseiwit (het gids-RNA) als ‘voorbeeld’ alles aan stukken knipt wat overeenkomt met dat gids-RNA. Virus af door zijdeur.
Lab
Zo gebeurt het in het echt. In het lab zijn er wat dingen versleuteld aan het systeem. De eerste stap is om gids-RNA te ontwerpen dat overeenkomt met sequenties in een beoogd gen om, bijvoorbeeld een bepaalde sequentie weg te knippen. Dit gids-RNA doet samen met Cas9 (of een andere genschaar) het knipwerk. Cas9 en gids-RNA vormen een complex aan het eind waarvan het RNA een haarspeldvorm aanneemt waarmee het vast aan het eiwit zit. Het andere deel van het gids-RNA is er om de juiste DNA-sequentie op te zoeken.
Als dat gids-RNA/CAs9-complex eenmaal in de celkern is dan gaat het op zoek naar een ‘aanlegplaats’ (PAM gedoopt). PAM bestaat uit maar een paar DNA-letters (een van de basen A, C, G en T), maar daar legt Cas9 aan. Daardoor wordt de belendende sequentie gedestabiliseerd, waardoor een stukje van de dubbele DNA-helix loskomt. Daardoor krijgt het gids-RNA de gelegenheid te controleren of het complex op het juiste deel van DNA is gearriveerd. Als dat niet zo is dan gaat het stel door, indien ze op de juiste plek zijn aangekomen dan zorgt het gids-RNA er voor dat de genschaar het DNA in tweeën knipt.
Je kunt zo een gen eruit snijden. Het reparatiemechanisme van DNA zorgt er dan voor dat de losse eindjes weer aan elkaar worden geknoopt.
Je kunt echter ook op die plek een nieuw stuk DNA inbouwen. Daarbij maak je, overigens, dan weer gebruik van de vaardigheden van een virus om stukjes DNA in te bouwen. Dat nieuwe DNA is dan onderdeel van het DNA van het virus, dat, zoals dat heet, daarbij wel ‘kreupel’ is gemaakt en niets ernstigers kan verrichten dan het nbouwen van het gewenste stukje DNA.
Meer dan Cas9
Zoals al verklapt zijn er meer eiwitten dan Cas9 die dienst doen als genschaar. Zo is er Cas3. Onderzoekers gebruiken Cas3 om antibiotica te ontwikkelen die gericht bepaalde bacteriën uitschakelen terwijl ze de rest van je darmflora intact laten. Zo heb je een systeem dat Sherlock is genoemd en werkt met Cas13 dat aanlegt aan RNA. Dergelijke systemen worden gebruikt voor het diagnostiseren van virusinfecties. Vooralsnog is Cas9 echter de populairste genschaar bij onderzoekers.
CRISPR is niet volmaakt. Soms knipt de schaar op een verkeerde plek. Vooralsnog is dat een van de belangrijkste hinderpalen om genoombewerking vol in te zetten in de klinisch praktijk. Het is natuurlijk niet de bedoeling dat je het ene probleem oplost, maar daarmee een ander schept. En als het zover is zullen we ook van elkaar moeten weten waar we de schaar gaan inzetten. Vooralsnog lijkt die discussie het grote publiek nauwelijks te beroeren of misschien vindt dat grote publiek het allemaal wel best. Erfelijke ziektes uitbannen? Mooi toch?
Bron: Wired
